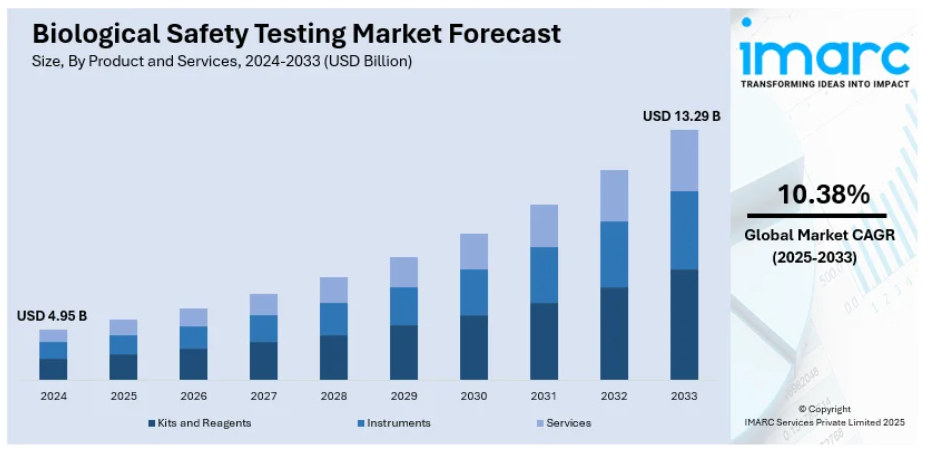
バイオ医薬品、ワクチン、バイオシミラーに対する需要の増加は、医療ニーズの高まりと慢性疾患の蔓延により、生物学的安全性試験市場を牽引しております。製品の安全性と有効性に関する厳格な規制ガイドライン、ならびにバイオテクノロジー研究開発への投資拡大が、市場の成長をさらに促進しております。細胞療法および遺伝子治療の進歩、ならびに受託研究機関(CRO)の拡大も、信頼性の高い安全性試験の需要を後押ししています。感染症の増加とパンデミック対策の必要性によりワクチン生産が加速し、厳格な安全性試験が求められています。自動化システムやハイスループットスクリーニングなどの試験技術の革新は、試験効率を向上させ、市場の拡大に寄与しています。製品品質に対する意識の高まりが、世界的な生物学的安全性試験市場の成長をさらに促進しています。
米国における生物学的安全性試験市場は、慢性疾患や感染症の増加に伴うバイオ医薬品、ワクチン、先進治療法への需要拡大に牽引されています。FDAをはじめとする規制当局の厳格な基準により、製品品質とコンプライアンスを確保するための包括的な安全性試験が必須となっています。米国は自動化やハイスループットシステムを含む革新的試験技術の採用においても主導的立場にあり、試験の精度と効率性を高めています。さらに、確立された製薬企業の存在、パンデミック対策への強い注力、契約研究機関(CRO)の成長などが、生物学的安全性試験市場の主要な動向として挙げられます。例えば、2024年10月には米国メリーランド州ロックビルにおいて、ドイツ・ダルムシュタットに本社を置くメルクKGaAのライフサイエンス部門であるミリポアシグマが、2億9000万ユーロを投じた新たな生物学的安全性試験施設を開設いたしました。従来型および革新的治療法において、生物安全性試験と分析開発は医薬品開発・商業化の必須要素です。これらのサービスに対する需要は世界的に二桁成長率で増加しています。この拡張により、同社は単一の統合ハブにおいて自動化と技術開発を推進可能となり、これは同社史上最大の受託試験分野への投資となります。
生物学的安全性試験市場の動向:
拡大する製薬・バイオテクノロジー分野
製薬およびバイオテクノロジー産業は、研究開発への投資増加により拡大を続けております。業界レポートによれば、2023年の世界の製薬分野における研究開発費は約3000億米ドルを超えました。複雑な疾患を含む様々な医療状態に対する医薬品、生物学的製剤、ワクチンの開発は、これらの分野が主導しております。その結果、徹底的な安全性評価の必要性が高まっており、患者の安全を確保するためには生物学的安全性試験が不可欠です。これは細菌、ウイルス、エンドトキシンなどの汚染物質に対する包括的な評価を含み、安全基準および法的要件への適合を保証します。同時に、疾患の進化する性質と製品の継続的な革新により、遺伝子治療や細胞治療などの新興療法に対する専門的な評価を含む安全性試験への高い需要が維持されており、生物学的安全性試験市場の需要に大きく寄与しています。
COVID-19パンデミックの影響
COVID-19パンデミックは、ワクチンや治療法の開発・導入を加速させることで産業に大きな影響を与えました。例えば、世界保健機関(WHO)によれば、2021年までに世界で130億回分以上のCOVID-19ワクチンが投与されています。これは厳格な安全性試験の重要性を浮き彫りにしました。これに加え、世界各国の政府および規制当局はこれらの製品に対する監視を強化し、ワクチン安全性評価、ウイルス検出アッセイ、COVID-19診断・治療薬の品質管理措置など、様々な試験サービスの需要急増を招きました。さらに、パンデミックは今後の健康危機への備えの必要性を強調することで産業の重点を変化させ、市場の拡大を維持しています。
規制順守への重視の高まり
世界の規制機関は、患者の安全と製品品質を重視し、バイオ医薬品に対する監視を強化しています。これらの規制は包括的な安全性評価を義務付けており、生物学的安全性試験は医薬品承認に不可欠な要素となっています。遺伝子治療や細胞治療などの先進医療用医薬品は、過去数年間で承認件数が増加しています。例えば、欧州医薬品庁の先進治療委員会は、2024年5月の総会において、重度および中等度のB型血友病治療薬であるDurveqtix(フィダナコゲン・エラパルボベック)に対し、肯定的な意見書草案を採択しました。これは、承認される先進治療医療製品(ATMP)の数が着実に増加しているという一般的な傾向の一部です。医薬品・バイオテクノロジー企業が製品承認と市場参入を得るために遵守すべき基準が厳格に変化する中、試験サービスの需要は高まっており、コンプライアンスにおける生物学的安全性試験の重要性が強調されています。さらに、遺伝子治療や細胞治療のような高度な治療法に対する規制の複雑化が進むにつれ、専門的な試験の必要性が浮き彫りになっています。専門的な評価がこれらの治療法の特有の特性に適応し、その有効性と安全性を保証しつつ変化する規制要件を満たすことで、市場の成長が維持されています。
生物安全性試験産業のセグメンテーション:
IMARC Groupは、市場レポートの各セグメントにおける主要トレンドの分析に加え、2025年から2033年までのグローバル、地域、国レベルでの予測を提供しております。当社のレポートでは、製品・サービス、試験タイプ、用途に基づいて市場を分類しております。
製品・サービス別分析:
- キット及び試薬
- 機器
- サービス
キット及び試薬は2024年に約41.3%の市場シェアを占め、市場をリードしております。分散型検査やポイントオブケア(POC)診断への傾向の高まりが、使いやすく携帯可能な検査キットの需要を促進しており、これが生物学的安全性試験の需要を牽引する主要因の一つとなっております。これらのキットは、特に資源が限られた環境において、医療従事者が迅速かつ効率的に安全性評価を実施することを可能にします。これと相まって、ゲノミクス、プロテオミクス、細胞培養を含むライフサイエンス分野における研究開発活動の拡大は、様々な用途向けの高品質な試験用試薬およびキットの継続的な供給を必要とし、市場の成長を促進しています。さらに、生物学的汚染物質が重大なリスクをもたらす可能性のある食品・飲料(F&B)産業において、製品の品質と安全性の確保への関心が高まっていることも、微生物学的分析用の試験キットおよび試薬の需要を押し上げ、市場の拡大に寄与しています。
試験種類別分析:
- エンドトキシン試験
- 無菌試験
- 細胞株認証および特性評価試験
- バイオバーデン試験
- 残留宿主汚染物質検出試験
- 外来性病原体検出試験
- その他
エンドトキシン試験は、2024年に約24.9%の市場シェアを占め、市場をリードしています。医療機器や医薬品製品の安全性と有効性を確保する重要な必要性により主に推進されるエンドトキシン検査の需要増加が、世界の生物学的安全性試験市場を強化しています。グラム陰性菌の細胞壁に存在する有毒物質であるエンドトキシンは、人体に導入されると深刻な健康上の合併症を引き起こす可能性があります。インプラントや薬物送達システムを含む医療機器の複雑さと多様性の増加は、潜在的な患者リスクを軽減するためにエンドトキシンに対する厳格な試験を必要としています。さらに、遺伝子治療やモノクローナル抗体などの個別化医薬品やバイオ医薬品への注目が高まる中、これらの先進的治療法の純度と安全性を保証するためには、綿密なエンドトキシン試験が求められており、市場を強化しています。これに加え、世界中の規制当局が厳格なエンドトキシン制限値の遵守を義務付けているため、医薬品製造や医療における正確で信頼性の高いエンドトキシン試験の需要が高まり、市場の成長を後押ししています。
用途別分析:
- ワクチン開発
- 血液製剤試験
- 細胞・遺伝子治療
- 組織および組織関連製品試験
- 幹細胞研究
ワクチン開発は2024年に約28.7%の市場シェアを占め、市場を牽引しています。ワクチン開発における生物学的安全性試験の需要は、安全かつ効果的なワクチンに対する世界的な緊急の必要性によって主に推進されています。COVID-19パンデミックを含む様々な感染症やウイルス発生に直面する中、ワクチン開発への注目はかつてないほど高まっています。規制当局は、ワクチンが効果的であるだけでなく有害な汚染物質を含まないことを保証するため、包括的な安全性評価を求めています。生物学的安全性試験はこのプロセスにおいて重要な役割を果たし、ワクチン候補物質の潜在的なウイルス・微生物汚染物質の評価、エンドトキシン不存在の確認、そしてヒト使用における総合的な安全性の評価を含みます。さらに、mRNAベースのワクチンなどの新規ワクチン技術の出現は、専門的な安全性評価を必要とし、生物学的安全性試験サービスへの需要増加に寄与しています。ワクチン安全性へのこの高まる重視は、世界規模での公衆衛生を守る上で、このような試験が果たす重要な役割を浮き彫りにしています。
地域別分析
- 北米
- アメリカ合衆国
- カナダ
- ヨーロッパ
- ドイツ
- フランス
- イギリス
- イタリア
- スペイン
- ロシア
- その他
- アジア太平洋
- 中国
- 日本
- インド
- 韓国
- オーストラリア
- インドネシア
- その他
- ラテンアメリカ
- ブラジル
- メキシコ
- その他
- 中東・アフリカ
2024年、北米は38.8%を超える最大の市場シェアを占めました。北米地域は、研究開発に重点を置いた強固な製薬・バイオテクノロジー産業を有しております。新薬、生物学的製剤、医療機器の絶え間ない革新と導入は、厳格な安全性評価を必要とし、生物学的安全性試験サービスの需要を牽引しております。これに加え、FDA(米国食品医薬品局)やその他の規制機関が定める厳格な基準に支配された同地域の積極的な規制環境は、包括的な安全性評価を義務付けており、市場の成長をさらに促進しております。さらに、COVID-19パンデミックなどの公衆衛生上の脅威に対抗する継続的な取り組みにより、ワクチン開発と試験の需要が高まっております。特に北米では、数多くの製薬会社や研究機関がワクチン研究・生産に積極的に関与しております。これらの要因に加え、同地域の先進的な医療インフラと製品品質・安全性に対する意識の高まりが相まって、北米の生物学的安全性試験市場の拡大を継続的に後押ししております。
主要地域別要点:
米国生物学的安全性試験市場分析
2024年、米国は北米地域において88.60%超の最大市場シェアを占めました。医薬品開発の増加や生物学的製剤に基づく治療法の台頭に伴い、米国の生物学的安全性試験に関連する成長要素が増加しています。2023年だけでも、FDAは新規承認薬55品目中25の生物学的製剤を承認しました。このうち12品目はモノクローナル抗体(mAbs)、5品目は酵素またはタンパク質製剤でした。産業報告書によれば、2024年1月時点で米国では20,465件の臨床試験が患者を受け入れており、これは生物学的製剤の安全性試験に対する需要の高まりを臨床的に示しています。チャールズリバーラボラトリーズやウーシー・アプテックといった主要ベンダー企業は、試験技術の進化に注力しております。遺伝子治療やワクチンに対する高度な安全性試験の強い要請が、市場成長をさらに加速させています。インビトロ試験と自動化への注目の高まりも、市場の効率性向上に寄与しています。技術の進歩により試験精度が向上し、所要時間が短縮される一方、安全性規制要件の高水準化が継続的にイノベーションを推進しており、米国は生物学的安全性試験分野におけるヨーロッパにおける主要プレイヤーとしての地位を確立しています。
ヨーロッパにおける生物学的安全性試験市場分析
ヨーロッパにおいても、強力な規制枠組みと安全な医薬品・生物学的製剤への需要増加により、生物学的安全性試験市場は成長を続けています。最近の産業レポートによれば、ヨーロッパ製薬業界の収益は2022年に既に3,000億ユーロ(3,090億米ドル)を突破しており、安全性試験ソリューションへの高い需要を生み出しています。ドイツとスイスは強力な市場貢献国であり、製薬業界をリードするロシュ社とバイエル社は常に自社製品の生物学的安全性に関心を寄せています。具体的には、欧州医薬品庁(EMA)などの規制機関が試験基準を強化したことで、高品質な生物学的試験サービスが発展しました。臨床研究や遺伝子治療の需要増加、バイオシミラーの重要性高まりが市場需要を牽引しています。さらに、精密検査と連動した個別化医療の概念が台頭し、地域の安全性試験サービス提供者の競争環境を変化させています。自動化技術やAI技術の活用拡大により、試験の効率性も向上しています。
アジア太平洋地域の生物学的安全性試験市場分析
アジア太平洋地域の生物学的安全性試験市場は、バイオテクノロジーへの投資増加および製薬製造の拡大により急速に成長しています。業界レポートによれば、中国の医薬品市場は2023年に1,600億米ドル規模に達し、これに伴い生物学的製剤の需要も高まっています。高齢化が進む人口増加に伴い、同地域への国家投資は多国籍企業にとって魅力的であり、例えばラボコープやバイオメリューといった企業が研究開発費の増加を背景に事業拡大を進めています。ハイスループット試験や次世代シーケンシングといった先進技術が地域のバイオテクノロジー分野で採用され、より高度な安全性試験環境が構築されています。さらに、同地域の強力な製造能力と費用対効果の高い試験ソリューションが相まって、世界的な生物学的安全性試験分野における重要なプレイヤーとしての地位を確立しています。
ラテンアメリカにおける生物学的安全性試験市場分析
ラテンアメリカの生物学的安全性試験市場も成長を続けており、これは医薬品生産の拡大と、安全に関する国際基準への準拠への注力の深化によって牽引されています。この成長を牽引しているのはブラジルであり、同国の生物製剤生産能力のさらなる拡大に伴い、生物学的安全性試験サービスへの需要増加が確認できます。アルゼンチンとメキシコも、医薬品製造能力の向上に向けた投資を通じて成長に貢献しています。産業レポートによれば、2024年4月時点でブラジルは地域最多となる約10,000件の臨床試験を実施しており、メキシコが約5,000件で次ぐ規模です。これは臨床研究と生物学的安全性の重要性への依存度の高さを示しています。ブラジル規制当局ANVISAの試験要件はさらに厳格化しており、新たな国際基準を満たすための高度な安全性試験への需要増加につながっています。さらに、需要増に対応するための試験サービスやインフラ強化への現地メーカーの投資が市場の拡大に直接寄与し、同地域を世界的な生物学的安全性試験市場においてますます重要な位置づけにしています。
中東・アフリカ生物学的安全性試験市場分析
中東・アフリカ地域では、多くの国々における医療投資と医薬品生産の増加を背景に、生物学的安全性試験市場が急成長しています。サウジアラビアの防衛支出(医療・医薬品安全対策費を含む)が市場拡大を牽引しています。アラブ首長国連邦(UAE)の医薬品市場は成長段階を維持しており、生物学的安全性試験が急速に重点分野となりつつあります。南アフリカは主要なバイオ製造拠点の一つとして台頭しています。国内の生物学的製剤生産は著しい成長を見せています。WHO国際臨床試験登録プラットフォームによれば、2022年時点で中東地域では4,593件、アフリカでは861件の臨床試験が実施されており、臨床研究と生物学的安全性の需要が高まっています。同地域における医療施設の増加と臨床試験の拡大により、生物学的安全性試験サービスの需要はさらに高まる見込みです。試験サービスは今後5年間で年率10%の成長が見込まれます。この傾向は、地方政府による医療水準とインフラの改善努力によってさらに後押しされています。
競争環境:
世界の生物学的安全性試験市場における主要企業間の激しい競争は、医薬品、生物学的製剤、医療機器の品質と安全性を保証する上でこの分野が果たす重要な役割に起因しています。この競争環境において、主要企業は市場地位を維持するため、サービスポートフォリオや地理的範囲を拡大する合併・買収・提携など様々な戦略を展開しております。さらに、研究開発への投資を通じて最先端の試験技術や手順を導入することで、産業動向を先取りすることも可能です。遺伝子治療や細胞治療などの個別化医療や先進治療への注目が高まる中、専門的な安全性試験サービスを特化して提供する企業には成長の機会が生まれています。全体として、世界の生物学的安全性試験市場の競争環境は、既存の主要企業間のダイナミックな相互作用によって特徴づけられています。
本市場調査レポートでは、競争環境に関する包括的な分析を提供しております。主要企業の詳細なプロファイルも併せて掲載しております。市場における主要企業の一部は以下の通りです:
- Avance Biosciences
- Charles River Laboratories
- Creative Biogene
- Eurofins Scientific
- Lonza Group AG
- Maravai LifeSciences
- Pace Analytical Services Inc.
- Pacific BioLabs
- Sartorius AG
- SGS SA
- ViruSure GmbH (Asahi Kasei Corporation)
- WuXi Biologics
(なお、これは主要プレイヤーの一部リストに過ぎず、完全なリストは報告書に記載されております。)
最近の動向:
- 2024年11月: マラヴァイ・ライフサイエンシズは、オフィシナエ・バイオ社からDNAおよびRNAを購入する意向を発表しました。これにより、マラヴァイ傘下のトライリンク・バイオテクノロジー社におけるmRNA製造能力が強化され、核酸研究が加速されます。オフィシナエ・バイオ社のAIベース技術は、革新的な核酸ベース療法および生物学的製剤の安全性試験に有用です。
- 2024年9月:ユーロフィンズはモダン・テスティング・サービス(MTS)の買収を発表しました。この買収により、消費財産業における生物学的安全性試験能力の強化が図られます。戦略的拡大により、ユーロフィンズS&L-T&Hのグローバルネットワークが強化され、MTSの専門知識を活用しながら、20カ国35ヶ所以上に広がる試験・検査・認証サービスが提供されます。
- 2024年7月: SGS北米は、リンカーンシャー・センター・オブ・エクセレンスにおける生物製剤試験サービスを拡充いたしました。新たな開発には、機器、科学的専門知識、ならびに新規生物製剤およびバイオシミラーの特性評価を支援する能力が含まれます。これら全てにより、バイオ医薬品企業様の試験プロセスが円滑化され、製品の安全性に関する全ての規制要件を満たすことが保証されます。
- 2024年6月:チャールズリバーラボラトリーズは、マテック社との共同研究により、in vitro吸入毒性試験法の開発に向け130万米ドルの助成金を獲得しました。本プロジェクトは、動物実験への依存度を最小限に抑えつつ、マテック社及び他パートナーが開発したEpiAirway™モデルを活用し、エアロゾル物質試験における新手法(NAM)の推進を目的としています。
- 2024年2月: クリエイティブバイオジェン社は、生物学的製剤中の望ましくない微生物の確実な検出に特化した、微生物試験における検証用微生物計数プラットフォームを開発したと発表しました。これにより安全性および効率性がさらに向上します。その柔軟性により、多様な顧客ニーズに合わせた特注ソリューションを提供します。
ステークホルダーにとっての主な利点:
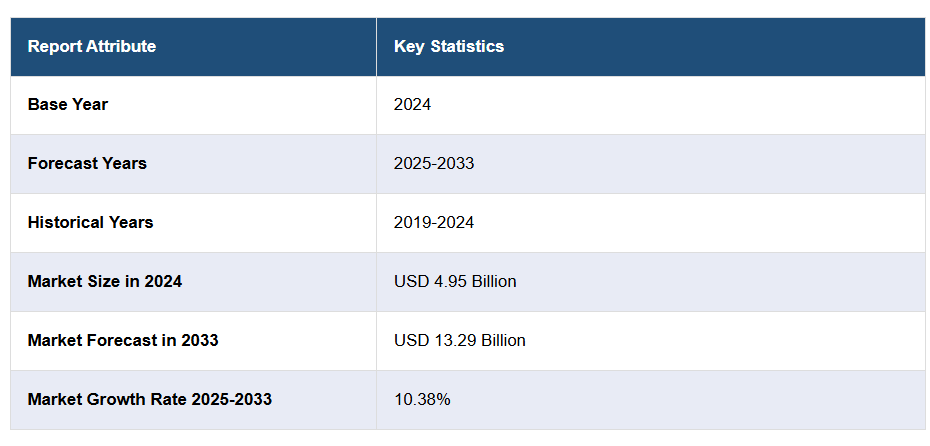
- IMARCの産業レポートは、2019年から2033年までの生物学的安全性試験市場について、様々な市場セグメント、過去および現在の市場動向、市場予測、市場力学に関する包括的な定量分析を提供します。
- 本調査レポートは、世界の生物学的安全性試験市場における最新の市場推進要因、課題、機会に関する情報を提供します。
- 本調査は、主要な地域市場と最も急成長している地域市場をマッピングします。さらに、各地域内の主要な国別市場を特定することを可能にします。
- ポーターの5つの力分析は、新規参入の影響、競争の激しさ、供給者の力、購買者の力、代替品の脅威を評価する上でステークホルダーを支援します。これにより、生物学的安全性試験産業内の競争レベルとその魅力を分析することが可能となります。
- 競争環境分析により、ステークホルダーは自社の競争環境を理解し、市場における主要プレイヤーの現在のポジションに関する洞察を得ることができます。
1 はじめに
2 調査範囲と方法論
2.1 本調査の目的
2.2 関係者
2.3 データソース
2.3.1 一次情報源
2.3.2 二次情報源
2.4 市場推定手法
2.4.1 ボトムアップアプローチ
2.4.2 トップダウンアプローチ
2.5 予測手法
3 エグゼクティブサマリー
4 はじめに
4.1 概要
4.2 主要な産業動向
5 世界の生物学的安全性試験市場
5.1 市場概要
5.2 市場実績
5.3 COVID-19の影響
5.4 市場予測
6 製品およびサービス別の市場区分
6.1 キットおよび試薬
6.1.1 市場動向
6.1.2 市場予測
6.2 機器
6.2.1 市場動向
6.2.2 市場予測
6.3 サービス
6.3.1 市場動向
6.3.2 市場予測
7 試験の種類別市場分析
7.1 エンドトキシン試験
7.1.1 市場動向
7.1.2 市場予測
7.2 無菌性試験
7.2.1 市場動向
7.2.2 市場予測
7.3 細胞株認証および特性評価試験
7.3.1 市場動向
7.3.2 市場予測
7.4 バイオバーデン試験
7.4.1 市場動向
7.4.2 市場予測
7.5 残留宿主汚染物質検出試験
7.5.1 市場動向
7.5.2 市場予測
7.6 外来異物検出試験
7.6.1 市場動向
7.6.2 市場予測
7.7 その他
7.7.1 市場動向
7.7.2 市場予測
8 用途別市場分析
8.1 ワクチン開発
8.1.1 市場動向
8.1.2 市場予測
8.2 血液製剤検査
8.2.1 市場動向
8.2.2 市場予測
8.3 細胞・遺伝子治療
8.3.1 市場動向
8.3.2 市場予測
8.4 組織および組織関連製品検査
8.4.1 市場動向
8.4.2 市場予測
8.5 幹細胞研究
8.5.1 市場動向
8.5.2 市場予測
9 地域別市場分析
9.1 北米
9.1.1 アメリカ合衆国
9.1.1.1 市場動向
9.1.1.2 市場予測
9.1.2 カナダ
9.1.2.1 市場動向
9.1.2.2 市場予測
9.2 アジア太平洋地域
9.2.1 中国
9.2.1.1 市場動向
9.2.1.2 市場予測
9.2.2 日本
9.2.2.1 市場動向
9.2.2.2 市場予測
9.2.3 インド
9.2.3.1 市場動向
9.2.3.2 市場予測
9.2.4 韓国
9.2.4.1 市場動向
9.2.4.2 市場予測
9.2.5 オーストラリア
9.2.5.1 市場動向
9.2.5.2 市場予測
9.2.6 インドネシア
9.2.6.1 市場動向
9.2.6.2 市場予測
9.2.7 その他
9.2.7.1 市場動向
9.2.7.2 市場予測
9.3 ヨーロッパ
9.3.1 ドイツ
9.3.1.1 市場動向
9.3.1.2 市場予測
9.3.2 フランス
9.3.2.1 市場動向
9.3.2.2 市場予測
9.3.3 イギリス
9.3.3.1 市場動向
9.3.3.2 市場予測
9.3.4 イタリア
9.3.4.1 市場動向
9.3.4.2 市場予測
9.3.5 スペイン
9.3.5.1 市場動向
9.3.5.2 市場予測
9.3.6 ロシア
9.3.6.1 市場動向
9.3.6.2 市場予測
9.3.7 その他
9.3.7.1 市場動向
9.3.7.2 市場予測
9.4 ラテンアメリカ
9.4.1 ブラジル
9.4.1.1 市場動向
9.4.1.2 市場予測
9.4.2 メキシコ
9.4.2.1 市場動向
9.4.2.2 市場予測
9.4.3 その他
9.4.3.1 市場動向
9.4.3.2 市場予測
9.5 中東およびアフリカ
9.5.1 市場動向
9.5.2 国別市場内訳
9.5.3 市場予測
10 SWOT分析
10.1 概要
10.2 強み
10.3 弱み
10.4 機会
10.5 脅威
11 バリューチェーン分析
12 ポーターの5つの力分析
12.1 概要
12.2 買い手の交渉力
12.3 供給者の交渉力
12.4 競争の激しさ
12.5 新規参入の脅威
12.6 代替品の脅威
13 価格分析
14 競争環境
14.1 市場構造
14.2 主要企業
14.3 主要企業の概要
14.3.1 アバンセ・バイオサイエンシズ
14.3.1.1 会社概要
14.3.1.2 製品ポートフォリオ
14.3.1.3 SWOT 分析
14.3.2 Charles River Laboratories
14.3.2.1 会社概要
14.3.2.2 製品ポートフォリオ
14.3.2.3 SWOT 分析
14.3.3 Creative Biogene
14.3.3.1 会社概要
14.3.3.2 製品ポートフォリオ
14.3.3.3 SWOT 分析
14.3.4 ユーロフィンズ・サイエンティフィック
14.3.4.1 会社概要
14.3.4.2 製品ポートフォリオ
14.3.4.3 SWOT 分析
14.3.5 ロンザ・グループ AG
14.3.5.1 会社概要
14.3.5.2 製品ポートフォリオ
14.3.5.3 SWOT 分析
14.3.6 マラヴァイ・ライフサイエンシズ
14.3.6.1 会社概要
14.3.6.2 製品ポートフォリオ
14.3.6.3 SWOT 分析
14.3.7 ペース・アナリティカル・サービス社
14.3.7.1 会社概要
14.3.7.2 製品ポートフォリオ
14.3.7.3 SWOT 分析
14.3.8 パシフィック・バイオラボ
14.3.8.1 会社概要
14.3.8.2 製品ポートフォリオ
14.3.8.3 SWOT 分析
14.3.9 Sartorius AG
14.3.9.1 会社概要
14.3.9.2 製品ポートフォリオ
14.3.9.3 SWOT 分析
14.3.10 SGS SA
14.3.10.1 会社概要
14.3.10.2 製品ポートフォリオ
14.3.10.3 SWOT 分析
14.3.11 ViruSure GmbH (旭化成株式会社)
14.3.11.1 会社概要
14.3.11.2 製品ポートフォリオ
14.3.11.3 SWOT 分析
14.3.12 WuXi Biologics
14.3.12.1 会社概要
14.3.12.2 製品ポートフォリオ
14.3.12.3 SWOT分析
図表一覧
図1:グローバル:生物学的安全性試験市場:主な推進要因と課題
図2:グローバル:生物学的安全性試験市場:売上高(10億米ドル)、2019-2024年
図3:世界:生物学的安全性試験市場予測:売上高(10億米ドル)、2025-2033年
図4:世界:生物学的安全性試験市場:製品・サービス別内訳(%)、2024年
図5:世界:生物学的安全性試験市場:試験種類別内訳(%)、2024年
図6:グローバル:生物学的安全性試験市場:用途別内訳(%)、2024年
図7:グローバル:生物学的安全性試験市場:地域別内訳(%)、2024年
図8:グローバル:生物学的安全性試験(キットおよび試薬)市場:売上高(百万米ドル)、2019年および2024年
図9:グローバル:生物学的安全性試験(キットおよび試薬)市場予測:売上高(百万米ドル)、2025-2033年
図10:グローバル:生物学的安全性試験(機器)市場:売上高(百万米ドル)、2019年および2024年
図11:世界:生物学的安全性試験(機器)市場予測:売上高(百万米ドル)、2025-2033年
図12:世界:生物学的安全性試験(サービス)市場:売上高(百万米ドル)、2019年及び2024年
図13:世界:生物学的安全性試験(サービス)市場予測:売上高(百万米ドル)、2025-2033年
図14:世界:生物学的安全性試験(エンドトキシン試験)市場:売上高(百万米ドル)、2019年及び2024年
図15:グローバル:生物学的安全性試験(エンドトキシン試験)市場予測:売上高 (百万米ドル)、2025-2033年
図16:グローバル:生物学的安全性試験(無菌試験)市場:売上高(百万米ドル)、2019年及び2024年
図17:グローバル:生物学的安全性試験(無菌試験)市場予測:売上高(百万米ドル)、2025-2033年
図18:世界:生物学的安全性試験(細胞株認証および特性評価試験)市場:売上高(百万米ドル)、2019年および2024年
図19:世界:生物学的安全性試験(細胞株認証および特性評価試験)市場予測:売上高(百万米ドル)、2025-2033年
図20:グローバル:生物学的安全性試験(バイオバーデン試験)市場:売上高(百万米ドル)、2019年及び2024年
図21:グローバル:生物学的安全性試験(バイオバーデン試験)市場予測:売上高(百万米ドル)、2025年~2033年
図22:グローバル:生物学的安全性試験(残留宿主汚染物質検出試験)市場:売上高(百万米ドル)、2019年および2024年
図23:世界:生物学的安全性試験(残留宿主汚染物質検出試験)市場予測:売上高(百万米ドル)、2025-2033年
図24:世界:生物学的安全性試験(外来性病原体検出試験)市場:売上高(百万米ドル)、2019年及び2024年
図25:世界:生物学的安全性試験(外来性病原体検出試験)市場予測:売上高(百万米ドル)、2025-2033年
図26:世界:生物学的安全性試験(その他の試験種類)市場:売上高(百万米ドル)、2019年及び2024年
図27:世界:生物学的安全性試験(その他の試験種類)市場予測:売上高(百万米ドル)、2025-2033年
図28:世界:生物学的安全性試験(ワクチン開発)市場:売上高(百万米ドル)、2019年及び2024年
図29:グローバル:生物学的安全性試験(ワクチン開発)市場予測:売上高(百万米ドル)、2025-2033年
図30:世界:生物学的安全性試験(血液製剤試験)市場:売上高(百万米ドル)、2019年及び2024年
図31:世界:生物学的安全性試験(血液製剤試験)市場予測:売上高(百万米ドル)、2025-2033年
図32:グローバル:生物学的安全性試験(細胞・遺伝子治療)市場:売上高(百万米ドル)、2019年及び2024年
図33:グローバル:生物学的安全性試験(細胞・遺伝子治療)市場予測:売上高(百万米ドル)、2025-2033年
図34:世界:生物学的安全性試験(組織および組織関連製品試験)市場:売上高(百万米ドル)、2019年および2024年
図35:世界:生物学的安全性試験(組織および組織関連製品試験)市場予測:売上高(百万米ドル)、2025年~2033年
図36:グローバル:生物学的安全性試験(幹細胞研究)市場:売上高(百万米ドル)、2019年及び2024年
図37:グローバル:生物学的安全性試験(幹細胞研究)市場予測:売上高(百万米ドル)、2025年~2033年
図38:北米:生物学的安全性試験市場:売上高(百万米ドル)、2019年及び2024年
図39:北米:生物学的安全性試験市場予測:売上高(百万米ドル)、2025-2033年
図40:米国:生物学的安全性試験市場:売上高(百万米ドル)、2019年及び2024年
図41:米国:生物学的安全性試験市場予測:売上高(百万米ドル)、2025-2033年
図42:カナダ:生物学的安全性試験市場:売上高(百万米ドル)、2019年及び2024年
図43:カナダ:生物学的安全性試験市場予測:売上高(百万米ドル)、2025-2033年
図44:アジア太平洋地域:生物学的安全性試験市場:売上高(百万米ドル)、2019年及び2024年
図45: アジア太平洋地域:生物安全試験市場予測:売上高(百万米ドル)、2025-2033年
図46:中国:生物安全試験市場:売上高(百万米ドル)、2019年及び2024年
図47:中国:生物安全試験市場予測:売上高(百万米ドル)、2025-2033年
図48:日本:生物学的安全性試験市場:売上高(百万米ドル)、2019年及び2024年
図49:日本:生物学的安全性試験市場予測:売上高(百万米ドル)、2025年~2033年
図50:インド:生物学的安全性試験市場:売上高(百万米ドル)、2019年及び2024年
図51:インド:生物学的安全性試験市場予測:売上高(百万米ドル)、2025-2033年
図52:韓国:生物学的安全性試験市場:売上高(百万米ドル)、2019年及び2024年
図53:韓国:生物学的安全性試験市場予測:売上高(百万米ドル)、2025-2033年
図54:オーストラリア:生物学的安全性試験市場:売上高(百万米ドル)、2019年及び2024年
図55:オーストラリア:生物学的安全性試験市場予測:売上高(百万米ドル)、2025-2033年
図56:インドネシア:生物学的安全性試験市場:売上高(百万米ドル)、2019年及び2024年
図57:インドネシア:生物学的安全性試験市場予測:売上高(百万米ドル)、2025年~2033年
図58:その他地域:生物学的安全性試験市場:売上高(百万米ドル)、2019年及び2024年
図59:その他地域:生物学的安全性試験市場予測:売上高(百万米ドル)、2025年~2033年
図60:ヨーロッパ:生物学的安全性試験市場:売上高(百万米ドル)、2019年及び2024年
図61:ヨーロッパ:生物学的安全性試験市場予測:売上高(百万米ドル)、2025-2033年
図62:ドイツ:生物学的安全性試験市場:売上高(百万米ドル)、2019年及び2024年
図63:ドイツ:生物学的安全性試験市場予測:売上高(百万米ドル)、2025-2033年
図64:フランス:生物学的安全性試験市場:売上高(百万米ドル)、2019年及び2024年
図65:フランス:生物学的安全性試験市場予測:売上高(百万米ドル)、2025-2033年
図66:英国:生物学的安全性試験市場:売上高(百万米ドル)、2019年及び2024年
図67:英国:生物学的安全性試験市場予測:売上高(百万米ドル)、2025-2033年
図68:イタリア:生物学的安全性試験市場:売上高(百万米ドル)、2019年及び2024年
図69:イタリア:生物学的安全性試験市場予測:売上高(百万米ドル)、2025-2033年
図70:スペイン:生物学的安全性試験市場:売上高(百万米ドル)、2019年及び2024年
図71:スペイン:生物学的安全性試験市場予測:売上高(百万米ドル)、2025-2033年
図72:ロシア:生物学的安全性試験市場:売上高(百万米ドル)、2019年及び2024年
図73:ロシア:生物学的安全性試験市場予測:売上高(百万米ドル)、2025年~2033年
図74:その他:生物学的安全性試験市場:売上高(百万米ドル)、2019年及び2024年
図75:その他地域:生物学的安全性試験市場予測:売上高(百万米ドル)、2025-2033年
図76:ラテンアメリカ:生物学的安全性試験市場:売上高(百万米ドル)、2019年及び2024年
図77:ラテンアメリカ:生物学的安全性試験市場予測:売上高(百万米ドル)、2025-2033年
図78:ブラジル:生物学的安全性試験市場:売上高(百万米ドル)、2019年及び2024年
図79:ブラジル:生物学的安全性試験市場予測:売上高(百万米ドル)、2025-2033年
図80:メキシコ:生物学的安全性試験市場:売上高(百万米ドル)、2019年及び2024年
図81:メキシコ:生物学的安全性試験市場予測:売上高(百万米ドル)、2025-2033年
図82:その他地域:生物学的安全性試験市場:売上高(百万米ドル)、2019年及び2024年
図83:その他地域:生物学的安全性試験市場予測:売上高(百万米ドル)、2025年~2033年
図84:中東・アフリカ:生物学的安全性試験市場:売上高(百万米ドル)、2019年及び2024年
図85:中東・アフリカ地域:生物学的安全性試験市場:国別内訳(%)、2024年
図86:中東・アフリカ地域:生物学的安全性試験市場予測:売上高(百万米ドル)、2025-2033年
図87:グローバル:生物学的安全性試験産業:SWOT分析
図88:グローバル:生物学的安全性試験産業:バリューチェーン分析
図89:グローバル:生物学的安全性試験産業:ポーターの5つの力分析
表一覧
表1:グローバル:生物学的安全性試験市場:主要産業ハイライト、2024年および2033年
表2:グローバル:生物学的安全性試験市場予測:製品およびサービス別内訳(百万米ドル)、2025-2033年
表3:グローバル:生物学的安全性試験市場予測:試験の種類別内訳(単位:百万米ドル)、2025-2033年
表4:グローバル:生物学的安全性試験市場予測:用途別内訳(百万米ドル)、2025-2033年
表5:グローバル:生物学的安全性試験市場予測:地域別内訳(百万米ドル)、2025-2033年
表6:グローバル:生物学的安全性試験市場:競争構造
表7:グローバル:生物学的安全性試験市場:主要企業
❖ 免責事項 ❖
http://www.globalresearch.jp/disclaimer












