❖本調査レポートの見積依頼/サンプル/購入/質問フォーム❖
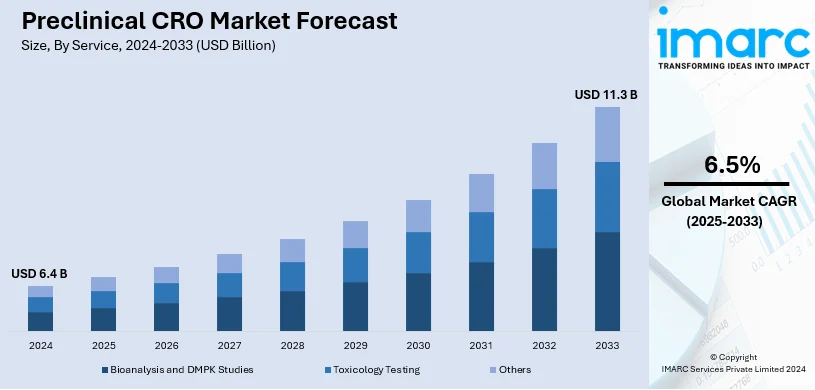
世界の非臨床CRO(医薬品開発業務受託機関)市場は、2024年に64億米ドルと評価され、2033年までに113億米ドルに達すると予測されており、2025年から2033年にかけて年平均成長率(CAGR)6.5%で成長する見込みです。地域別では北米が市場を支配し、2024年には47.5%以上の市場シェアを占めています。特に米国では約93.7%の市場シェアを持つ巨大な市場が形成されており、研究開発(R&D)支出の増加、規制環境の複雑化、企業のコアコンピテンシーへの集中、専門治療法の進歩が市場を牽引しています。
非臨床CRO市場成長の主な原動力は、医薬品発見の効率化とコスト削減を目的としたR&Dアウトソーシング需要の拡大です。製薬・バイオテクノロジー企業は、CROの専門知識、先進技術、包括的な非臨床試験サービスへの依存度を高めています。さらに、広範なバイオ医薬品研究、革新的な治療法への投資増加、厳格な規制要件への対応も市場成長を促進しています。慢性疾患の蔓延と医薬品開発の加速も、非臨床CROサービスの需要を高める要因です。人工知能(AI)を活用した創薬やラボ作業の改善といった継続的な技術進歩も、CROとの提携をより効率的かつ魅力的なものにしています。
米国では、慢性疾患の罹患率の高さが非臨床CROの市場需要をさらに押し上げています。疾病対策センター(CDC)の統計によると、米国の成人10人中6人が癌、心臓病、糖尿病などの慢性疾患を抱えており、これらは米国の主要な死因となっています。新たな治療法の必要性が市場成長を強化しています。また、医薬品開発の複雑化と規制要件の厳格化により、企業はCROの専門知識を求めるようになっています。
市場トレンドとしては、製薬・バイオテクノロジー産業におけるR&D活動の活発化が挙げられます。現代の医薬品開発プロセスは複雑で、新薬の安全性と有効性を確認するために長期間にわたる非臨床試験が必要です。研究者は、米国食品医薬品局(FDA)の規制に定められた優良試験所規範(GLP)を遵守する必要があります。インドの非臨床CRO市場も急速に成長しており、2023年には1億8330万米ドルと評価され、2030年までにCAGR 11.4%で成長すると予測されています。SyngeneやJubilant Biosysのような企業が毒性学、安全性薬理学、バイオ分析サービスで革新を推進しています。CROへの非臨床R&D活動のアウトソーシングは、社内で行うよりも費用対効果が高いとされています。例えば、2024年1月には、国立トランスレーショナル科学振興センター(NCATS)が他のNIH機関と協力して非臨床研究ツールボックスを開発しました。
製薬・バイオテクノロジー産業における複雑な規制環境も、非臨床CRO市場の重要な推進要因です。FDAや欧州医薬品庁(EMA)などの規制機関は、新薬の安全性と有効性を実証するために広範な非臨床試験を要求します。新薬が研究室から市場に出るまでには最大15年かかることもあり、規制要件への準拠を確実にするために非臨床CROサービスの需要が高まっています。また、臨床試験のグローバル化に伴い、製薬企業は各国の複雑な規制状況を理解する必要があり、国際的な規制要件に精通したCROが企業を支援します。
医薬品開発コストの上昇も、非臨床CRO市場の収益を押し上げています。新薬の発見は非常に複雑で時間のかかるプロセスであり、広範な研究と試験が不可欠です。非臨床試験の実施に伴う高コストは、この複雑さに起因します。EMAとFDAは新薬の安全性と有効性を確立するために完全な非臨床試験を要求しており、これらの規制要件を満たすことは高コストです。医薬品開発は本質的にリスクが高く、多額の投資にもかかわらず多くの医薬品が市場に到達できません。成功する医薬品を開発するには10年から15年かかり、失敗の40%から50%はヒトでの望ましい効果の欠如、約10%から15%は薬物動態特性の不備、約30%は制御不能な毒性によるものです。CROは非臨床研究に関する専門知識を提供することで、これらのリスクを軽減し、検討すべき医薬品の選択をより適切に導くことができます。
非臨床CRO市場は、サービス、最終用途、地域に基づいて分類されます。サービス別では、毒性試験が最大のセグメントであり、市場の約51.6%を占めています。その他には、バイオ分析およびDMPK(薬物動態・代謝)研究などが含まれます。
2024年の前臨床CRO市場は、医薬品の安全性保証と厳格な規制基準遵守における毒性試験の重要性により成長しています。革新的な治療法の需要増加、医薬品製剤の複雑化、慢性疾患の発生率増加、バイオ医薬品研究への投資拡大が、市場を牽引する主要因です。毒性試験は、前臨床CRO市場における中核的なサービスとなっています。
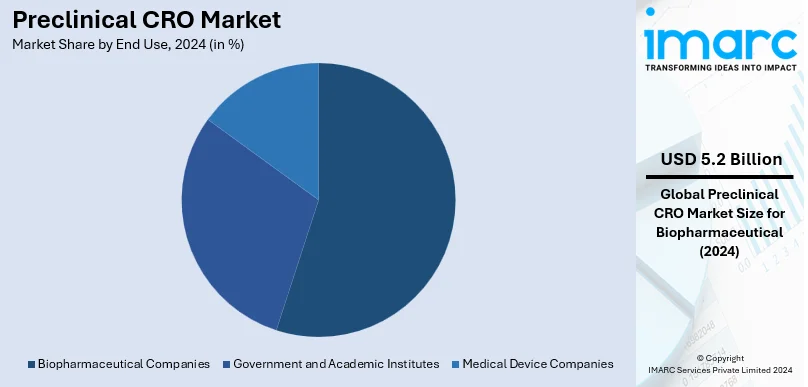
エンドユーザー別では、バイオ医薬品企業が2024年に市場シェアの約81.0%を占める最大の利用者です。生物製剤や標的療法には広範な前臨床研究が不可欠であり、これらの企業は高度な試験能力、規制要件への対応、運用コスト削減、市場投入期間短縮のためCROサービスを積極的に活用しています。慢性疾患の増加と個別化医療への需要も、バイオ医薬品企業による投資を促進し、市場成長の主要な推進力となっています。
地域別では、北米が2024年に約47.5%のシェアで最大市場です。製薬・バイオテクノロジー産業の強さ、高い研究助成金、確立された規制枠組みが背景にあります。米国は、最先端の医療インフラ、慢性疾患の蔓延、AI駆動型創薬やラボ自動化といった先進技術の普及により、成長を牽引しています。バイオ医薬品企業は、コストと時間節約のためアウトソーシングを増やしており、北米は前臨床CRO活動の主要ハブとしての地位を強化しています。例えば、米国製薬産業は強力なR&D投資と世界市場での優位性を通じてCRO採用を推進し、カリフォルニア州での個別化医療、マサチューセッツ州での腫瘍学研究などがリーダーシップを示しています。
欧州も前臨床CRO市場で重要な地位を占め、高度な医療インフラとバイオテクノロジー・製薬イノベーションに注力しています。ドイツ、英国、フランスが主要貢献国であり、強固な規制枠組みと合理化された承認プロセスが魅力です。ドイツの国家製薬戦略は、承認迅速化や現地研究奨励を通じて、臨床試験シェアの回復を目指しています。AIの創薬への統合や精密医療研究が進展し、ドイツは毒性学・薬物動態研究を、英国はCROと学術センターの連携を強化しています。スイスやベルギーも専門サービスを提供し、地域の能力を高めています。
アジア太平洋地域は、バイオテクノロジーの進歩、革新的な創薬、費用対効果の高い研究ソリューションへの需要増加により、世界的リーダーとして台頭しています。中国、インド、韓国、シンガポールは、強固なインフラ、熟練した労働力、有利な規制枠組みにより、前臨床アウトソーシングのハブとなっています。2017年から2021年にかけて世界の臨床試験の50%以上を牽引したこの地域は、低コスト、豊富な施設、合理化された規制プロセスが特徴です。中国のAI統合による精密医療研究加速、インドの費用対効果の高いサービス、韓国の免疫腫瘍学試験への注力などが、地域の強みです。
ラテンアメリカも、生物医学研究とイノベーションの進歩により、前臨床CROのダイナミックなハブとして浮上しています。
前臨床CRO市場は、専門サービス需要と医薬品開発アウトソーシングの増加により、激しい競争が特徴です。主要企業は包括的サービス、先進技術、グローバル展開で市場を牽引し、研究開発、戦略的提携、買収に投資しています。中小CROもニッチサービス、費用対効果、柔軟性で存在感を増し、AIや自動化プラットフォームによるイノベーションが競争の鍵です。地域プレイヤーは新興市場で拡大しています。
ラテンアメリカでは、ブラジル、メキシコ、アルゼンチンが最先端施設、競争力のあるコスト、熟練した専門家を活用し、グローバル協力を誘致。ブラジルでは2022年に62万5千件のがん症例があったにもかかわらず、世界のがん臨床試験の2.2%しか実施されておらず、試験制限、規制遅延、リソース不足に対処する前臨床CROの必要性が高まっています。これにより、CRO採用を通じた腫瘍学研究におけるブラジルの役割が拡大。北米市場に近い戦略的立地も魅力で、メキシコは毒性学、ブラジルは薬物動態学に特化し、地域は世界の前臨床研究の重要プレイヤーとなっています。
中東およびアフリカ地域では、前臨床CROの採用がヘルスケアイノベーションにおける地位を向上させています。UAE、サウジアラビア、南アフリカはCROサービスを活用し、医薬品開発と研究能力を強化。2023年に360億米ドルの中東製薬市場は、投資増加と規制要件によりCRO採用を促進。高度な研究サービスへの注力は、コスト削減、タイムライン短縮、競争優位性をもたらし、ドバイやケープタウンが研究ハブ化しています。
最近の動向として、2024年9月にPharmaLegacyがBTS Researchを買収し北米での前臨床サービスを強化。同年9月にはCROパートナー選定戦略に関する記事が発表されました。4月にはLabCorpが精密腫瘍学ポートフォリオを強化し、3月にはVeeda Clinical Researchが欧州の腫瘍学専門CROであるHeadsを買収。1月にはNCATSとNIHが創薬を効率化する包括的な前臨床研究ツールボックスを作成しました。
本レポートは、2019年から2033年までの前臨床CRO市場の定量的分析を提供し、市場の推進要因、課題、機会に関する最新情報を提供します。主要な地域市場および国レベルの市場を特定し、ポーターのファイブフォース分析を通じて競争環境を評価します。主要企業にはCharles River Laboratories Inc.、Covance Inc.、Eurofins Scientific、ICON Plc、MD Biosciences Inc.、Medpace、Parexel International Corporation、PPD Inc.、Wuxi AppTecなどが含まれます。
1 序文
2 範囲と方法論
2.1 調査目的
2.2 関係者
2.3 データソース
2.3.1 一次情報源
2.3.2 二次情報源
2.4 市場推定
2.4.1 ボトムアップアプローチ
2.4.2 トップダウンアプローチ
2.5 予測方法論
3 エグゼクティブサマリー
4 はじめに
4.1 概要
4.2 主要な業界トレンド
5 世界の前臨床CRO市場
5.1 市場概要
5.2 市場実績
5.3 COVID-19の影響
5.4 市場予測
6 サービス別市場内訳
6.1 バイオアナリシスおよびDMPK研究
6.1.1 市場トレンド
6.1.2 市場予測
6.2 毒性試験
6.2.1 市場トレンド
6.2.2 市場予測
6.3 その他
6.3.1 市場トレンド
6.3.2 市場予測
7 用途別市場内訳
7.1 バイオ医薬品企業
7.1.1 市場トレンド
7.1.2 市場予測
7.2 政府および学術機関
7.2.1 市場トレンド
7.2.2 市場予測
7.3 医療機器企業
7.3.1 市場トレンド
7.3.2 市場予測
8 地域別市場内訳
8.1 北米
8.1.1 米国
8.1.1.1 市場トレンド
8.1.1.2 市場予測
8.1.2 カナダ
8.1.2.1 市場トレンド
8.1.2.2 市場予測
8.2 アジア太平洋
8.2.1 中国
8.2.1.1 市場トレンド
8.2.1.2 市場予測
8.2.2 日本
8.2.2.1 市場トレンド
8.2.2.2 市場予測
8.2.3 インド
8.2.3.1 市場トレンド
8.2.3.2 市場予測
8.2.4 韓国
8.2.4.1 市場トレンド
8.2.4.2 市場予測
8.2.5 オーストラリア
8.2.5.1 市場トレンド
8.2.5.2 市場予測
8.2.6 インドネシア
8.2.6.1 市場トレンド
8.2.6.2 市場予測
8.2.7 その他
8.2.7.1 市場トレンド
8.2.7.2 市場予測
8.3 ヨーロッパ
8.3.1 ドイツ
8.3.1.1 市場トレンド
8.3.1.2 市場予測
8.3.2 フランス
8.3.2.1 市場トレンド
8.3.2.2 市場予測
8.3.3 イギリス
8.3.3.1 市場トレンド
8.3.3.2 市場予測
8.3.4 イタリア
8.3.4.1 市場トレンド
8.3.4.2 市場予測
8.3.5 スペイン
8.3.5.1 市場トレンド
8.3.5.2 市場予測
8.3.6 ロシア
8.3.6.1 市場トレンド
8.3.6.2 市場予測
8.3.7 その他
8.3.7.1 市場トレンド
8.3.7.2 市場予測
8.4 ラテンアメリカ
8.4.1 ブラジル
8.4.1.1 市場トレンド
8.4.1.2 市場予測
8.4.2 メキシコ
8.4.2.1 市場トレンド
8.4.2.2 市場予測
8.4.3 その他
8.4.3.1 市場トレンド
8.4.3.2 市場予測
8.5 中東およびアフリカ
8.5.1 市場トレンド
8.5.2 国別市場内訳
8.5.3 市場予測
9 SWOT分析
9.1 概要
9.2 強み
9.3 弱み
9.4 機会
9.5 脅威
10 バリューチェーン分析
11 ポーターのファイブフォース分析
11.1 概要
11.2 買い手の交渉力
11.3 供給者の交渉力
11.4 競争の程度
11.5 新規参入の脅威
11.6 代替品の脅威
12 価格分析
13 競争環境
13.1 市場構造
13.2 主要企業
13.3 主要企業のプロファイル
13.3.1 Charles River Laboratories Inc.
13.3.1.1 会社概要
13.3.1.2 製品ポートフォリオ
13.3.1.3 財務状況
13.3.1.4 SWOT分析
13.3.2 Covance Inc. (Laboratory Corporation of America Holdings)
13.3.2.1 会社概要
13.3.2.2 製品ポートフォリオ
13.3.2.3 SWOT分析
13.3.3 Eurofins Scientific
13.3.3.1 会社概要
13.3.3.2 製品ポートフォリオ
13.3.4 ICON Plc
13.3.4.1 会社概要
13.3.4.2 製品ポートフォリオ
13.3.4.3 財務状況
13.3.4.4 SWOT分析
13.3.5 MD Biosciences Inc. (MLM Medical Labs)
13.3.5.1 会社概要
13.3.5.2 製品ポートフォリオ
13.3.6 Medpace
13.3.6.1 会社概要
13.3.6.2 製品ポートフォリオ
13.3.6.3 財務状況
13.3.6.4 SWOT分析
13.3.7 Parexel International Corporation
13.3.7.1 会社概要
13.3.7.2 製品ポートフォリオ
13.3.7.3 SWOT分析
13.3.8 PPD Inc.
13.3.8.1 会社概要
13.3.8.2 製品ポートフォリオ
13.3.8.3 財務状況
13.3.8.4 SWOT分析
13.3.9 Wuxi AppTec
13.3.9.1 会社概要
13.3.9.2 製品ポートフォリオ
13.3.9.3 財務状況
図のリスト
図1:世界の非臨床CRO市場:主要な推進要因と課題
図2:世界の非臨床CRO市場:販売額(10億米ドル)、2019-2024年
図3:世界の非臨床CRO市場予測:販売額(10億米ドル)、2025-2033年
図4:世界の非臨床CRO市場:サービス別内訳(%)、2024年
図5:世界の非臨床CRO市場:最終用途別内訳(%)、2024年
図6:世界の非臨床CRO市場:地域別内訳(%)、2024年
図7:世界の非臨床CRO(バイオアナリシスおよびDMPK研究)市場:販売額(百万米ドル)、2019年および2024年
図8:世界の非臨床CRO(バイオアナリシスおよびDMPK研究)市場予測:販売額(百万米ドル)、2025-2033年
図9:世界の非臨床CRO(毒性試験)市場:販売額(百万米ドル)、2019年および2024年
図10:世界の非臨床CRO(毒性試験)市場予測:販売額(百万米ドル)、2025-2033年
図11:世界の非臨床CRO(その他のサービス)市場:販売額(百万米ドル)、2019年および2024年
図12:世界の非臨床CRO(その他のサービス)市場予測:販売額(百万米ドル)、2025-2033年
図13:世界の非臨床CRO(バイオ医薬品企業)市場:販売額(百万米ドル)、2019年および2024年
図14:世界の非臨床CRO(バイオ医薬品企業)市場予測:販売額(百万米ドル)、2025-2033年
図15:世界の非臨床CRO(政府および学術機関)市場:販売額(百万米ドル)、2019年および2024年
図16:世界の非臨床CRO(政府および学術機関)市場予測:販売額(百万米ドル)、2025-2033年
図17:世界の非臨床CRO(医療機器企業)市場:販売額(百万米ドル)、2019年および2024年
図18:世界の非臨床CRO(医療機器企業)市場予測:販売額(百万米ドル)、2025-2033年
図19:北米の非臨床CRO市場:販売額(百万米ドル)、2019年および2024年
図20:北米の非臨床CRO市場予測:販売額(百万米ドル)、2025-2033年
図21:米国:前臨床CRO市場:売上高(百万米ドル)、2019年・2024年
図22:米国:前臨床CRO市場予測:売上高(百万米ドル)、2025年~2033年
図23:カナダ:前臨床CRO市場:売上高(百万米ドル)、2019年・2024年
図24:カナダ:前臨床CRO市場予測:売上高(百万米ドル)、2025年~2033年
図25:アジア太平洋:前臨床CRO市場:売上高(百万米ドル)、2019年・2024年
図26:アジア太平洋:前臨床CRO市場予測:売上高(百万米ドル)、2025年~2033年
図27:中国:前臨床CRO市場:売上高(百万米ドル)、2019年・2024年
図28:中国:前臨床CRO市場予測:売上高(百万米ドル)、2025年~2033年
図29:日本:前臨床CRO市場:売上高(百万米ドル)、2019年・2024年
図30:日本:前臨床CRO市場予測:売上高(百万米ドル)、2025年~2033年
図31:インド:前臨床CRO市場:売上高(百万米ドル)、2019年・2024年
図32:インド:前臨床CRO市場予測:売上高(百万米ドル)、2025年~2033年
図33:韓国:前臨床CRO市場:売上高(百万米ドル)、2019年・2024年
図34:韓国:前臨床CRO市場予測:売上高(百万米ドル)、2025年~2033年
図35:オーストラリア:前臨床CRO市場:売上高(百万米ドル)、2019年・2024年
図36:オーストラリア:前臨床CRO市場予測:売上高(百万米ドル)、2025年~2033年
図37:インドネシア:前臨床CRO市場:売上高(百万米ドル)、2019年・2024年
図38:インドネシア:前臨床CRO市場予測:売上高(百万米ドル)、2025年~2033年
図39:その他:前臨床CRO市場:売上高(百万米ドル)、2019年・2024年
図40:その他:前臨床CRO市場予測:売上高(百万米ドル)、2025年~2033年
図41:欧州:前臨床CRO市場:売上高(百万米ドル)、2019年・2024年
図42:欧州:前臨床CRO市場予測:売上高(百万米ドル)、2025年~2033年
図43:ドイツ:前臨床CRO市場:売上高(百万米ドル)、2019年・2024年
図44:ドイツ:前臨床CRO市場予測:売上高(百万米ドル)、2025年~2033年
図45:フランス:前臨床CRO市場:売上高(百万米ドル)、2019年・2024年
図46:フランス:前臨床CRO市場予測:売上高(百万米ドル)、2025年~2033年
図47:英国:前臨床CRO市場:売上高(百万米ドル)、2019年・2024年
図48:英国:前臨床CRO市場予測:売上高(百万米ドル)、2025年~2033年
図49:イタリア:前臨床CRO市場:売上高(百万米ドル)、2019年・2024年
図50:イタリア:前臨床CRO市場予測:売上高(百万米ドル)、2025年~2033年
図51:スペイン:前臨床CRO市場:売上高(百万米ドル)、2019年・2024年
図52:スペイン:前臨床CRO市場予測:売上高(百万米ドル)、2025年~2033年
図53:ロシア:前臨床CRO市場:売上高(百万米ドル)、2019年・2024年
図54:ロシア:前臨床CRO市場予測:売上高(百万米ドル)、2025年~2033年
図55:その他:前臨床CRO市場:売上高(百万米ドル)、2019年・2024年
図56:その他:前臨床CRO市場予測:売上高(百万米ドル)、2025年~2033年
図57:ラテンアメリカ:前臨床CRO市場:売上高(百万米ドル)、2019年・2024年
図58:ラテンアメリカ:前臨床CRO市場予測:売上高(百万米ドル)、2025年~2033年
図59:ブラジル:前臨床CRO市場:売上高(百万米ドル)、2019年・2024年
図60:ブラジル:前臨床CRO市場予測:売上高(百万米ドル)、2025年~2033年
図61:メキシコ:前臨床CRO市場:売上高(百万米ドル)、2019年・2024年
図62:メキシコ:前臨床CRO市場予測:売上高(百万米ドル)、2025年~2033年
図63:その他:前臨床CRO市場:売上高(百万米ドル)、2019年・2024年
図64:その他:前臨床CRO市場予測:売上高(百万米ドル)、2025年~2033年
図65: 中東・アフリカ: 前臨床CRO市場: 販売額(百万米ドル)、2019年および2024年
図66: 中東・アフリカ: 前臨床CRO市場: 国別内訳(%)、2024年
図67: 中東・アフリカ: 前臨床CRO市場予測: 販売額(百万米ドル)、2025年~2033年
図68: 世界: 前臨床CRO産業: SWOT分析
図69: 世界: 前臨床CRO産業: バリューチェーン分析
図70: 世界: 前臨床CRO産業: ポーターのファイブフォース分析

前臨床CRO(Contract Research Organization)は、医薬品、バイオテクノロジー製品、医療機器などの開発において、ヒトでの臨床試験を開始する前段階の研究開発活動を外部委託で支援する専門機関でございます。主に、新規薬物の探索、非臨床安全性評価、薬効薬理試験などを実施し、規制当局への申請に必要な科学的データを提供いたします。これにより、製薬企業やバイオベンチャーは、自社リソースを補完し、開発プロセスを効率化することが可能となります。
提供するサービス内容によって、前臨床CROは多岐にわたります。例えば、薬物の作用機序や有効性を評価する薬理試験CRO、薬物の安全性(急性毒性、反復投与毒性、遺伝毒性、がん原性など)を評価し、GLP(優良試験所規範)に準拠した試験を実施する毒性試験CROがございます。また、薬物の体内での吸収、分布、代謝、排泄(ADME)を詳細に解析する薬物動態試験(DMPK)CRO、生体試料中の薬物や代謝物の濃度を測定するバイオアナリシスCRO、組織学的評価を通じて薬物の影響を解析する病理試験CRO、薬物の最適な製剤化を支援する製剤開発CROなどもございます。さらに、特定の疾患領域(例:がん、神経疾患)に特化したCROや、げっ歯類・非げっ歯類動物を用いた試験に特化したCROも存在し、クライアントの多様なニーズに応えています。
前臨床CROの利用は、製薬企業やバイオベンチャーにとって非常に重要な戦略的選択肢でございます。専門的な知識と設備を活用することで、研究開発期間の短縮とコスト削減に貢献し、開発の効率化と加速を実現いたします。また、特定の試験や技術に関する高度な専門性を持つCROを利用することで、自社にないノウハウを補完し、開発初期段階での安全性や有効性の評価を徹底することで、後の臨床開発におけるリスクを低減いたします。GLPなどの厳格な規制基準に準拠した試験を実施し、国内外の規制当局への申請をサポートすることも重要な役割です。新薬探索における化合物のスクリーニングから、候補化合物の選定、最適化までを支援するほか、医療機器開発における生体適合性試験や安全性評価など、医療機器特有の非臨床試験も手掛けております。
前臨床CROでは、最新の科学技術が積極的に導入され、研究開発の質と効率の向上に貢献しています。例えば、多数の化合物を高速で評価し、有望な候補を効率的に特定するハイスループットスクリーニング(HTS)技術がございます。また、薬物の作用機序解明やバイオマーカー探索に利用されるゲノミクス、プロテオミクス、メタボロミクスなどのオミックス技術も不可欠です。生体内での薬物動態や病態変化を非侵襲的に評価するMRI、PET、CTなどの高度画像診断技術、疾患モデル動物の作製や遺伝子治療研究に応用されるCRISPR/遺伝子編集技術も活用されています。さらに、大量の実験データの解析、可視化、解釈に不可欠なバイオインフォマティクス、試験の再現性と効率性を向上させる自動化・ロボット技術、薬物毒性予測や候補化合物の選定、データ解析の最適化に活用されるAI/機械学習も、開発期間の短縮に大きく貢献しています。近年では、ヒトの臓器機能を模倣したマイクロ流体デバイスである臓器チップ(Organ-on-a-chip)も導入され、よりヒトに近い環境での薬物評価を可能にしています。