❖本調査レポートの見積依頼/サンプル/購入/質問フォーム❖
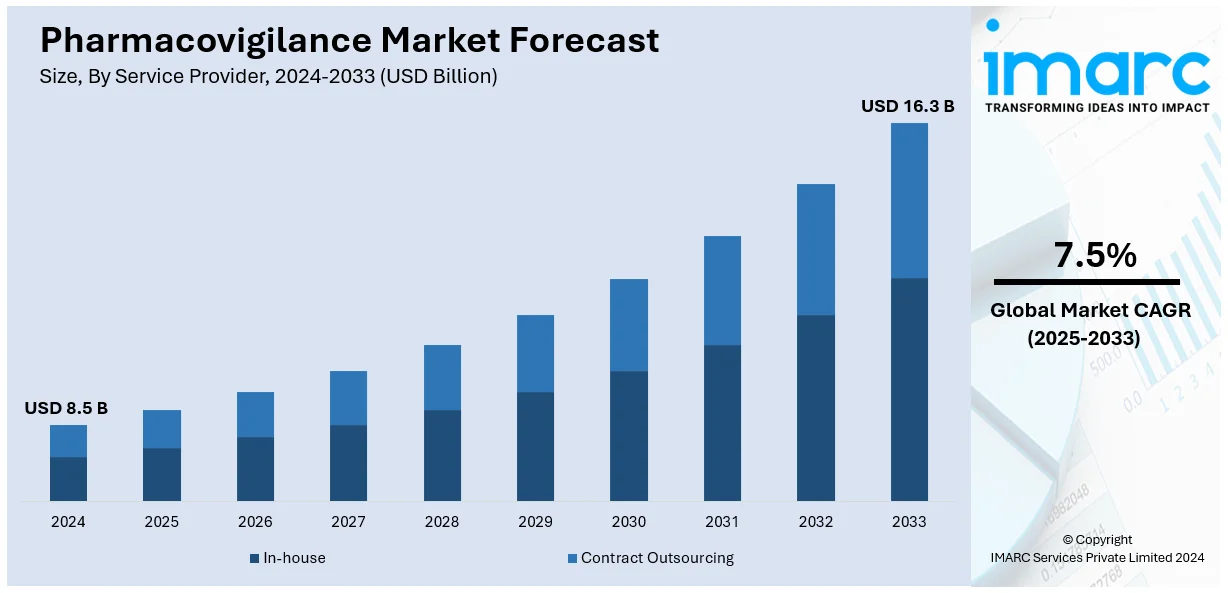
世界の医薬品安全性監視(ファーマコビジランス、PV)市場は、2025年に85億ドルと評価され、2034年には163億ドルに達し、2026年から2034年にかけて年平均成長率7.5%で成長すると予測されています。現在、北米が市場の33.7%を占め、優位な地位を確立しています。
この市場成長の主な要因は多岐にわたります。まず、医薬品の複雑化(バイオ医薬品、遺伝子治療、個別化医療など)が進み、世界的に規制が厳格化していることが挙げられます。また、AI、機械学習、自然言語処理、ビッグデータ分析といった先進技術の導入が、シグナル検出や医薬品安全性評価の効率を高め、市場拡大を後押ししています。欧州医薬品庁(EMA)がAIツールのガイドラインを発表するなど、技術活用への意欲も示されています。
さらに、多剤併用や薬物乱用による有害事象(ADR)の発生増加、製薬・バイオテクノロジー産業の成長、慢性疾患の増加と新薬上市の加速が、堅牢なPVシステムの需要を高めています。製薬企業が臨床および市販後の安全性管理を専門企業にアウトソーシングする傾向も顕著で、これにより運用コストを削減しつつ規制遵守を維持しています。
米国市場では、広範な製薬産業と多数の臨床試験がPV需要を牽引しています。バイオシミラーや個別化医療の台頭は、医薬品安全性評価の複雑性を増し、市場を活性化させています。米国食品医薬品局(FDA)のSentinel Initiativeのような政府の安全性監視推進策や、患者中心のアプローチによるリアルワールドデータ(RWD)収集の重視も市場成長に貢献しています。遠隔医療やデジタルヘルスツールの急速な採用は、ADRの遠隔報告・監視を促進しています。
PV市場の主要トレンドとしては、以下の点が挙げられます。
1. **技術革新によるPV業務の変革:** AI、ML、NLP、ビッグデータ分析がADR監視、シグナル検出、規制報告といった中核機能を高速かつ大規模に処理し、従来のPVモデルをデータリッチなエコシステムへと変革しています。SanofiとDeloitteのConvergeHEALTH Safetyプラットフォームや、ArisGlobalとUSFDAのFAERS IIシステム統合などがその例です。
2. **政府規制とリアルワールドエビデンス(RWE)の強化:** USFDA、EMAなどの規制機関は監視を強化し、特に新規医薬品や複雑な治療法の生産増加に伴い、安全性報告に関する厳格な義務を課しています。ニトロソアミン汚染による医薬品リコール事例は、厳格な試験基準が不可欠であることを示しています。市販後監視への依存度が高まり、RWEが臨床設定を超えた医薬品リスクプロファイルの更新に不可欠であると認識されています。
3. **医薬品の複雑化に伴うPVサービス需要の増加:** バイオ医薬品、遺伝子治療、個別化医療といった新薬開発の複雑化、慢性疾患や併存疾患の増加による多剤併用が、専門的な安全性監視サービスへの需要を高めています。製薬企業は、スケーラブルなインフラ、経験豊富なアナリスト、地域ごとの規制情報へのアクセスを提供する専門サービスプロバイダーにPV業務をアウトソーシングしており、これはコスト削減だけでなくパフォーマンス向上にも寄与しています。
4. **複雑な臨床試験と多剤併用が市場を牽引:** 2023年には22,000件以上の新規臨床試験が開始され、適応型プロトコルや分散型要素、患者中心設計が特徴となっています。これらのトレンドは、複数の地域でリアルタイムに機能する機敏でプロアクティブな安全性システムの必要性を強調しています。また、慢性疾患の増加に伴う多剤併用は、ADR監視をこれまで以上に重要にしています。分散型臨床試験プラットフォームとの連携(CognizantとMedableの協業など)により、安全性監視が効率化されています。
市場セグメンテーションでは、サービスプロバイダー別では契約アウトソーシングが61.2%の最大シェアを占めています。これは、費用対効果、規制要件への準拠、リスク監視における生産性、運用コスト回避、そして製薬企業が製品研究やマーケティングといった中核事業に集中できるためです。製品ライフサイクル別では、第IV相(市販後監視)が76.5%と最大の市場シェアを占めています。
医薬品承認後の安全性監視が極めて重要であるため、市販後調査(フェーズIV)はファーマコビジランス市場の成長を牽引する主要セグメントとなっています。規制要件の厳格化、有害事象(ADR)報告数の増加、新薬上市の活発化、リアルワールドエビデンス(RWE)とビッグデータ分析の統合、および専門サービスプロバイダーへのアウトソーシングの活用がこの成長を後押ししています。
タイプ別分析では、「自発報告」が31.9%のシェアで市場をリードしています。これは、比較的低コストかつ短時間でADRを特定できるためで、医療従事者や製薬企業に対し、FAERSのような中央リポジトリへのADR報告が義務付けられていること、国民の意識向上、および患者による直接報告の増加がその拡大を促進しています。機械学習(ML)や自然言語処理(NLP)といった先進技術の導入も、データ分析の精度を高めています。
プロセスフロー別分析では、「シグナル検出」が38.2%と最大のセグメントを占めています。これは、医薬品の開発段階から市販後に至るまで、安全性に関する懸念を特定し管理する上で中心的な役割を果たすためです。臨床試験データ、電子カルテ(EHR)、患者記録からのリアルタイムデータ収集がその基盤であり、機械学習(ML)アルゴリズムが有害事象分析の効率を大幅に向上させています。ビッグデータ分析やRWEの統合、医薬品開発プロジェクトの増加、薬の安全性に対する国民の意識向上により、シグナル検出は今後も力強い成長が見込まれます。
治療領域別分析では、「腫瘍学」が27.8%の最大シェアを占めています。腫瘍学は臨床試験および承認薬の数が最も多く、世界的ながん罹患率の増加(2040年には2,956万件と推定)が、腫瘍薬の開発と包括的な安全性対策の必要性を高めています。個別化医療や免疫療法は有害事象報告の複雑性を増し、ファーマコビジランスプロセスの活用を不可欠にしています。
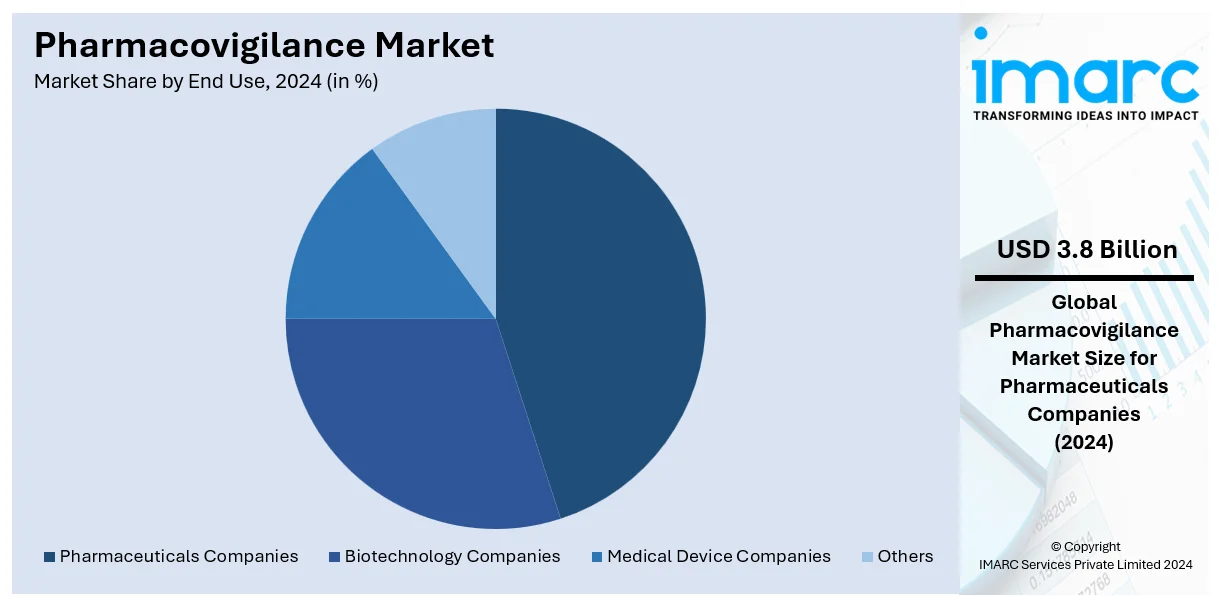
エンドユース別分析では、「製薬会社」が44.2%のシェアで最大のセグメントとなっています。製薬会社は医薬品開発と安全性において大きな責任を負い、規制要件を満たしADRのリスクを低減するために多額のファーマコビジランス費用を投じています。新規化学物質(NCE)や臨床試験の増加、個別化医療や生物学的製剤における追跡・リスク評価の複雑化が、AIなどの堅牢なツールの導入を促しています。
地域別分析では、「北米」が33.7%の最大シェアを占めています。これは、米国における高度な医療インフラ(例:6,120の病院と916,752床の病床)とFDAによる厳格な規制枠組みに起因しています。慢性疾患の有病率上昇と高齢化が医薬品消費を増加させ、効果的なファーマコビジランスの需要を高めています。北米はAIとビッグデータの統合においても先行しており、効率性とコンプライアンスを向上させています。
特に米国は2024年に北米ファーマコビジランス市場の83.40%を占め、FDAの厳格な規制、AIやML、自動化といった技術進歩、医療意識の向上が市場を牽引しています。米国保健福祉省によると、心臓病、がん、糖尿病などの主要な慢性疾患を抱える人口が推定1億2,900万人に上るため、継続的な医薬品安全性監視の需要が高まっており、EHRやウェアラブルデバイスの統合がリアルタイムデータ収集を可能にしています。
欧州市場も、欧州医薬品庁(EMA)および各国機関によって定められた効果的な規制枠組みに強く牽引されています。EUファーマコビジランス指令(2010/84/EU)が安全性監視と報告を強化し、患者安全への懸念、疾病の脅威、高齢化(2023年1月1日時点でEU人口4億4,880万人の5分の1以上が65歳以上)が医薬品の継続的な安全性評価の必要性を高めています。ビッグデータ、AI、EHRなどの現代技術の応用もファーマコビジランスの改善とADRの早期特定に貢献しており、アウトソーシングの傾向も見られます。
ファーマコビジランス市場は、医薬品産業の成長、薬剤消費の増加、慢性疾患の蔓延、そして薬物安全性とリスク管理への注力の高まりを背景に、世界的に急速な拡大を続けています。
アジア太平洋地域では、医薬品産業の成長、慢性疾患(高齢者の膝痛の有病率が中国で11~56%、日本で33%、韓国で38%、ベトナムで61%と報告)の増加、効果的な市販後調査の必要性が市場を牽引しています。中国やインドなどの新興市場では、医療インフラへの大規模な投資が進み、ファーマコビジランスデータの収集と分析が改善されています。また、臨床試験の増加や電子カルテ(EHR)などの技術進歩も市場成長を後押ししています。
ラテンアメリカ地域の市場は、規制遵守と薬物安全性監視への需要増が主な原動力です。医薬品部門の拡大と医療意識の向上に加え、ブラジルで年間約92万8千人が慢性疾患で死亡しているという報告が、効果的なファーマコビジランスシステムの必要性を浮き彫りにしています。ブラジルのANVISAやメキシコのCOFEPRISといった国家機関による規制強化、先進技術の導入、ファーマコビジランスサービスのアウトソーシングが市場成長に貢献しています。
中東・アフリカ地域では、規制の改善、医療インフラの拡充、薬物安全性への意識向上によって市場が形成されています。アラブ首長国連邦(UAE)では自己申告による慢性疾患の有病率が23.0%に達し、肥満、糖尿病、喘息/アレルギーが一般的であることから、患者の安全を確保するための堅牢なファーマコビジランスシステムへの需要が高まっています。医薬品市場の拡大と臨床試験の増加も、包括的な薬物安全性監視の必要性を増大させています。
競争環境は激化しており、主要企業は技術革新と戦略的パートナーシップを通じてサービス提供の向上に注力しています。AIや機械学習(ML)を活用した有害事象の自動検出や予測分析がトレンドとなっており、企業は運用コスト削減と高水準の維持を目指し、新興市場へのファーマコビジランスサービスのアウトソーシングを通じてグローバル展開を拡大しています。臨床研究機関(CRO)や医療提供者との戦略的提携も、データ収集と分析の効率化のために一般的になっています。さらに、リアルワールドエビデンス(RWE)や患者報告アウトカム(PRO)を安全評価に統合する動きも加速しており、薬物安全性と規制遵守の改善への業界のコミットメントを示しています。
最新の動向として、2025年4月にはELIQUENT Life SciencesがTruliant Consultingを買収し、製品ライフサイクル全体にわたるサポートを強化しました。2025年3月にはTech MahindraとNVIDIAがAIを活用したファーマコビジランスソリューションを共同開発し、ワークフローの自動化・最適化により、処理時間を40%短縮、データ精度を30%向上、運用コストを25%削減する成果を上げています。同月、ArisGlobalはAI駆動型新製品3種を発表し、LSK Global Pharma ServicesはOracle Argusを採用して薬物安全性分析を強化しました。2024年8月には、インドのファーマコビジランスプログラム(PvPI)が、患者、医師、看護師、製薬業界からの有害事象報告のための国内初の安全データベース「ADRMSソフトウェア」を立ち上げました。
本ファーマコビジランス市場調査レポートは、2020年から2034年までの市場セグメント、歴史的および現在の市場トレンド、市場予測、市場ダイナミクスに関する包括的な定量分析を提供します。市場の推進要因、課題、機会、主要な地域別・国別市場を網羅し、ポーターのファイブフォース分析や競争環境分析を通じて、市場の競争レベルと魅力を評価し、主要企業の現状を理解するのに役立ちます。
1 序文
2 範囲と方法論
2.1 調査目的
2.2 関係者
2.3 データソース
2.3.1 一次情報源
2.3.2 二次情報源
2.4 市場推定
2.4.1 ボトムアップアプローチ
2.4.2 トップダウンアプローチ
2.5 予測方法論
3 エグゼクティブサマリー
4 はじめに
4.1 概要
4.2 主要な業界トレンド
5 グローバルファーマコビジランス市場
5.1 市場概要
5.2 市場実績
5.3 COVID-19の影響
5.4 市場予測
6 サービスプロバイダー別市場内訳
6.1 社内
6.1.1 市場トレンド
6.1.2 市場予測
6.2 外部委託
6.2.1 市場トレンド
6.2.2 市場予測
7 製品ライフサイクル別市場内訳
7.1 前臨床
7.1.1 市場トレンド
7.1.2 市場予測
7.2 第I相
7.2.1 市場トレンド
7.2.2 市場予測
7.3 第II相
7.3.1 市場トレンド
7.3.2 市場予測
7.4 第III相
7.4.1 市場トレンド
7.4.2 市場予測
7.5 第IV相
7.5.1 市場トレンド
7.5.2 市場予測
8 タイプ別市場内訳
8.1 自発報告
8.1.1 市場トレンド
8.1.2 市場予測
8.2 強化されたADR報告
8.2.1 市場トレンド
8.2.2 市場予測
8.3 ターゲット型自発報告
8.3.1 市場トレンド
8.3.2 市場予測
8.4 コホートイベントモニタリング
8.4.1 市場トレンド
8.4.2 市場予測
8.5 EHRマイニング
8.5.1 市場トレンド
8.5.2 市場予測
9 プロセスフロー別市場内訳
9.1 症例データ管理
9.1.1 市場トレンド
9.1.2 主要な種類
9.1.2.1 症例記録
9.1.2.2 症例データ分析
9.1.2.3 医療レビューと報告
9.1.3 市場予測
9.2 シグナル検出
9.2.1 市場トレンド
9.2.2 主要な種類
9.2.2.1 有害事象記録
9.2.2.2 有害事象分析
9.2.2.3 有害事象レビューと報告
9.2.3 市場予測
9.3 リスク管理システム
9.3.1 市場トレンド
9.3.2 主要な種類
9.3.2.1 リスク評価システム
9.3.2.2 リスク軽減システム
9.3.3 市場予測
10 治療領域別市場内訳
10.1 腫瘍学
10.1.1 市場トレンド
10.1.2 市場予測
10.2 神経学
10.2.1 市場トレンド
10.2.2 市場予測
10.3 循環器学
10.3.1 市場トレンド
10.3.2 市場予測
10.4 呼吸器系
10.4.1 市場トレンド
10.4.2 市場予測
10.5 その他
10.5.1 市場トレンド
10.5.2 市場予測
11 最終用途別市場内訳
11.1 製薬会社
11.1.1 市場トレンド
11.1.2 市場予測
11.2 バイオテクノロジー企業
11.2.1 市場トレンド
11.2.2 市場予測
11.3 医療機器会社
11.3.1 市場トレンド
11.3.2 市場予測
11.4 その他
11.4.1 市場トレンド
11.4.2 市場予測
12 地域別市場内訳
12.1 北米
12.1.1 米国
12.1.1.1 市場トレンド
12.1.1.2 市場予測
12.1.2 カナダ
12.1.2.1 市場トレンド
12.1.2.2 市場予測
12.2 アジア太平洋
12.2.1 中国
12.2.1.1 市場動向
12.2.1.2 市場予測
12.2.2 日本
12.2.2.1 市場動向
12.2.2.2 市場予測
12.2.3 インド
12.2.3.1 市場動向
12.2.3.2 市場予測
12.2.4 韓国
12.2.4.1 市場動向
12.2.4.2 市場予測
12.2.5 オーストラリア
12.2.5.1 市場動向
12.2.5.2 市場予測
12.2.6 インドネシア
12.2.6.1 市場動向
12.2.6.2 市場予測
12.2.7 その他
12.2.7.1 市場動向
12.2.7.2 市場予測
12.3 欧州
12.3.1 ドイツ
12.3.1.1 市場動向
12.3.1.2 市場予測
12.3.2 フランス
12.3.2.1 市場動向
12.3.2.2 市場予測
12.3.3 イギリス
12.3.3.1 市場動向
12.3.3.2 市場予測
12.3.4 イタリア
12.3.4.1 市場動向
12.3.4.2 市場予測
12.3.5 スペイン
12.3.5.1 市場動向
12.3.5.2 市場予測
12.3.6 ロシア
12.3.6.1 市場動向
12.3.6.2 市場予測
12.3.7 その他
12.3.7.1 市場動向
12.3.7.2 市場予測
12.4 ラテンアメリカ
12.4.1 ブラジル
12.4.1.1 市場動向
12.4.1.2 市場予測
12.4.2 メキシコ
12.4.2.1 市場動向
12.4.2.2 市場予測
12.4.3 その他
12.4.3.1 市場動向
12.4.3.2 市場予測
12.5 中東およびアフリカ
12.5.1 市場動向
12.5.2 国別市場内訳
12.5.3 市場予測
13 SWOT分析
13.1 概要
13.2 強み
13.3 弱み
13.4 機会
13.5 脅威
14 バリューチェーン分析
15 ポーターの5つの力分析
15.1 概要
15.2 買い手の交渉力
15.3 供給者の交渉力
15.4 競争の度合い
15.5 新規参入の脅威
15.6 代替品の脅威
16 価格分析
17 競争環境
17.1 市場構造
17.2 主要企業
17.3 主要企業のプロファイル
17.3.1 アクセンチュア
17.3.1.1 企業概要
17.3.1.2 製品ポートフォリオ
17.3.1.3 財務状況
17.3.1.4 SWOT分析
17.3.2 アリスグローバル
17.3.2.1 企業概要
17.3.2.2 製品ポートフォリオ
17.3.3 バイオクリニカ (シンベン・パートナーズLLP)
17.3.3.1 企業概要
17.3.3.2 製品ポートフォリオ
17.3.3.3 SWOT分析
17.3.4 キャップジェミニ
17.3.4.1 企業概要
17.3.4.2 製品ポートフォリオ
17.3.5 コグニザント
17.3.5.1 企業概要
17.3.5.2 製品ポートフォリオ
17.3.5.3 財務状況
17.3.5.4 SWOT分析
17.3.6 インターナショナル・ビジネス・マシーンズ・コーポレーション
17.3.6.1 企業概要
17.3.6.2 製品ポートフォリオ
17.3.6.3 財務状況
17.3.6.4 SWOT分析
17.3.7 アイコン
17.3.7.1 企業概要
17.3.7.2 製品ポートフォリオ
17.3.7.3 財務状況
17.3.7.4 SWOT分析
17.3.8 IQVIA
17.3.8.1 会社概要
17.3.8.2 製品ポートフォリオ
17.3.8.3 財務状況
17.3.8.4 SWOT分析
17.3.9 ITClinical
17.3.9.1 会社概要
17.3.9.2 製品ポートフォリオ
17.3.10 Parexel International Corporation
17.3.10.1 会社概要
17.3.10.2 製品ポートフォリオ
17.3.10.3 SWOT分析
17.3.11 Wipro Limited
17.3.11.1 会社概要
17.3.11.2 製品ポートフォリオ
17.3.11.3 財務状況
17.3.11.4 SWOT分析
図目次
図1: グローバル: ファーマコビジランス市場: 主要な推進要因と課題
図2: グローバル: ファーマコビジランス市場: 売上高 (10億米ドル単位), 2020-2025年
図3: グローバル: ファーマコビジランス市場予測: 売上高 (10億米ドル単位), 2026-2034年
図4: グローバル: ファーマコビジランス市場: サービスプロバイダー別内訳 (%), 2025年
図5: グローバル: ファーマコビジランス市場: 製品ライフサイクル別内訳 (%), 2025年
図6: グローバル: ファーマコビジランス市場: タイプ別内訳 (%), 2025年
図7: グローバル: ファーマコビジランス市場: プロセスフロー別内訳 (%), 2025年
図8: グローバル: ファーマコビジランス市場: 治療領域別内訳 (%), 2025年
図9: グローバル: ファーマコビジランス市場: 最終用途別内訳 (%), 2025年
図10: グローバル: ファーマコビジランス市場: 地域別内訳 (%), 2025年
図11: グローバル: ファーマコビジランス (社内) 市場: 売上高 (100万米ドル単位), 2020年および2025年
図12: グローバル: ファーマコビジランス (社内) 市場予測: 売上高 (100万米ドル単位), 2026-2034年
図13: グローバル: ファーマコビジランス (契約アウトソーシング) 市場: 売上高 (100万米ドル単位), 2020年および2025年
図14: グローバル: ファーマコビジランス (契約アウトソーシング) 市場予測: 売上高 (100万米ドル単位), 2026-2034年
図15: グローバル: ファーマコビジランス (前臨床) 市場: 売上高 (100万米ドル単位), 2020年および2025年
図16: グローバル: ファーマコビジランス (前臨床) 市場予測: 売上高 (100万米ドル単位), 2026-2034年
図17: グローバル: ファーマコビジランス (第I相) 市場: 売上高 (100万米ドル単位), 2020年および2025年
図18: グローバル: ファーマコビジランス (第I相) 市場予測: 売上高 (100万米ドル単位), 2026-2034年
図19: グローバル: ファーマコビジランス (第II相) 市場: 売上高 (100万米ドル単位), 2020年および2025年
図20: グローバル: ファーマコビジランス (第II相) 市場予測: 売上高 (100万米ドル単位), 2026-2034年
図21: グローバル: ファーマコビジランス (第III相) 市場: 売上高 (100万米ドル単位), 2020年および2025年
図22: グローバル: ファーマコビジランス (第III相) 市場予測: 売上高 (100万米ドル単位), 2026-2034年
図23: グローバル: ファーマコビジランス (第IV相) 市場: 売上高 (100万米ドル単位), 2020年および2025年
図24: グローバル: ファーマコビジランス (第IV相) 市場予測: 売上高 (100万米ドル単位), 2026-2034年
図25: グローバル: ファーマコビジランス (自発報告) 市場: 売上高 (100万米ドル単位), 2020年および2025年
図26: グローバル: ファーマコビジランス (自発報告) 市場予測: 売上高 (100万米ドル単位), 2026-2034年
図27: グローバル: ファーマコビジランス (強化されたADR報告) 市場: 売上高 (100万米ドル単位), 2020年および2025年
図28: グローバル: ファーマコビジランス (強化されたADR報告) 市場予測: 売上高 (100万米ドル単位), 2026-2034年
図29: グローバル: ファーマコビジランス (標的型自発報告) 市場: 売上高 (100万米ドル単位), 2020年および2025年
図30: グローバル: ファーマコビジランス (標的型自発報告) 市場予測: 売上高 (100万米ドル単位), 2026-2034年
図31: グローバル: ファーマコビジランス (コホートイベントモニタリング) 市場: 売上高 (100万米ドル単位), 2020年および2025年
図32: グローバル: ファーマコビジランス (コホートイベントモニタリング) 市場予測: 売上高 (100万米ドル単位), 2026-2034年
図33: 世界: 医薬品安全性監視 (EHRマイニング) 市場: 販売額 (単位: 100万米ドル), 2020年および2025年
図34: 世界: 医薬品安全性監視 (EHRマイニング) 市場予測: 販売額 (単位: 100万米ドル), 2026年~2034年
図35: 世界: 医薬品安全性監視 (症例データ管理) 市場: 販売額 (単位: 100万米ドル), 2020年および2025年
図36: 世界: 医薬品安全性監視 (症例データ管理) 市場予測: 販売額 (単位: 100万米ドル), 2026年~2034年
図37: 世界: 医薬品安全性監視 (シグナル検出) 市場: 販売額 (単位: 100万米ドル), 2020年および2025年
図38: 世界: 医薬品安全性監視 (シグナル検出) 市場予測: 販売額 (単位: 100万米ドル), 2026年~2034年
図39: 世界: 医薬品安全性監視 (リスク管理システム) 市場: 販売額 (単位: 100万米ドル), 2020年および2025年
図40: 世界: 医薬品安全性監視 (リスク管理システム) 市場予測: 販売額 (単位: 100万米ドル), 2026年~2034年
図41: 世界: 医薬品安全性監視 (腫瘍領域) 市場: 販売額 (単位: 100万米ドル), 2020年および2025年
図42: 世界: 医薬品安全性監視 (腫瘍領域) 市場予測: 販売額 (単位: 100万米ドル), 2026年~2034年
図43: 世界: 医薬品安全性監視 (神経領域) 市場: 販売額 (単位: 100万米ドル), 2020年および2025年
図44: 世界: 医薬品安全性監視 (神経領域) 市場予測: 販売額 (単位: 100万米ドル), 2026年~2034年
図45: 世界: 医薬品安全性監視 (循環器領域) 市場: 販売額 (単位: 100万米ドル), 2020年および2025年
図46: 世界: 医薬品安全性監視 (循環器領域) 市場予測: 販売額 (単位: 100万米ドル), 2026年~2034年
図47: 世界: 医薬品安全性監視 (呼吸器系) 市場: 販売額 (単位: 100万米ドル), 2020年および2025年
図48: 世界: 医薬品安全性監視 (呼吸器系) 市場予測: 販売額 (単位: 100万米ドル), 2026年~2034年
図49: 世界: 医薬品安全性監視 (その他の治療領域) 市場: 販売額 (単位: 100万米ドル), 2020年および2025年
図50: 世界: 医薬品安全性監視 (その他の治療領域) 市場予測: 販売額 (単位: 100万米ドル), 2026年~2034年
図51: 世界: 医薬品安全性監視 (製薬会社) 市場: 販売額 (単位: 100万米ドル), 2020年および2025年
図52: 世界: 医薬品安全性監視 (製薬会社) 市場予測: 販売額 (単位: 100万米ドル), 2026年~2034年
図53: 世界: 医薬品安全性監視 (バイオテクノロジー企業) 市場: 販売額 (単位: 100万米ドル), 2020年および2025年
図54: 世界: 医薬品安全性監視 (バイオテクノロジー企業) 市場予測: 販売額 (単位: 100万米ドル), 2026年~2034年
図55: 世界: 医薬品安全性監視 (医療機器会社) 市場: 販売額 (単位: 100万米ドル), 2020年および2025年
図56: 世界: 医薬品安全性監視 (医療機器会社) 市場予測: 販売額 (単位: 100万米ドル), 2026年~2034年
図57: 世界: 医薬品安全性監視 (その他の最終用途) 市場: 販売額 (単位: 100万米ドル), 2020年および2025年
図58: 世界: 医薬品安全性監視 (その他の最終用途) 市場予測: 販売額 (単位: 100万米ドル), 2026年~2034年
図59: 北米: 医薬品安全性監視市場: 販売額 (単位: 100万米ドル), 2020年および2025年
図60: 北米: 医薬品安全性監視市場予測: 販売額 (単位: 100万米ドル), 2026年~2034年
図61: 米国: 医薬品安全性監視市場: 販売額 (単位: 100万米ドル), 2020年および2025年
図62: 米国: 医薬品安全性監視市場予測: 販売額 (単位: 100万米ドル), 2026年~2034年
図63: カナダ: 医薬品安全性監視市場: 販売額 (単位: 100万米ドル), 2020年および2025年
図64: カナダ: 医薬品安全性監視市場予測: 販売額 (単位: 100万米ドル), 2026年~2034年
図65: アジア太平洋: 医薬品安全性監視市場: 販売額 (単位: 100万米ドル), 2020年および2025年
図66: アジア太平洋: 医薬品安全性監視市場予測: 販売額 (単位: 100万米ドル), 2026年~2034年
図67: 中国: 医薬品安全性監視市場: 販売額 (単位: 100万米ドル), 2020年および2025年
図68: 中国: 医薬品安全性監視市場予測: 販売額 (単位: 100万米ドル), 2026年~2034年
図69: 日本: 医薬品安全性監視市場: 販売額 (単位: 100万米ドル), 2020年および2025年
図70: 日本: 医薬品安全性監視市場予測: 販売額 (単位: 100万米ドル), 2026年~2034年
図71:インド:医薬品安全性監視市場:販売額(百万米ドル)、2020年および2025年
図72:インド:医薬品安全性監視市場予測:販売額(百万米ドル)、2026年~2034年
図73:韓国:医薬品安全性監視市場:販売額(百万米ドル)、2020年および2025年
図74:韓国:医薬品安全性監視市場予測:販売額(百万米ドル)、2026年~2034年
図75:オーストラリア:医薬品安全性監視市場:販売額(百万米ドル)、2020年および2025年
図76:オーストラリア:医薬品安全性監視市場予測:販売額(百万米ドル)、2026年~2034年
図77:インドネシア:医薬品安全性監視市場:販売額(百万米ドル)、2020年および2025年
図78:インドネシア:医薬品安全性監視市場予測:販売額(百万米ドル)、2026年~2034年
図79:その他:医薬品安全性監視市場:販売額(百万米ドル)、2020年および2025年
図80:その他:医薬品安全性監視市場予測:販売額(百万米ドル)、2026年~2034年
図81:ヨーロッパ:医薬品安全性監視市場:販売額(百万米ドル)、2020年および2025年
図82:ヨーロッパ:医薬品安全性監視市場予測:販売額(百万米ドル)、2026年~2034年
図83:ドイツ:医薬品安全性監視市場:販売額(百万米ドル)、2020年および2025年
図84:ドイツ:医薬品安全性監視市場予測:販売額(百万米ドル)、2026年~2034年
図85:フランス:医薬品安全性監視市場:販売額(百万米ドル)、2020年および2025年
図86:フランス:医薬品安全性監視市場予測:販売額(百万米ドル)、2026年~2034年
図87:イギリス:医薬品安全性監視市場:販売額(百万米ドル)、2020年および2025年
図88:イギリス:医薬品安全性監視市場予測:販売額(百万米ドル)、2026年~2034年
図89:イタリア:医薬品安全性監視市場:販売額(百万米ドル)、2020年および2025年
図90:イタリア:医薬品安全性監視市場予測:販売額(百万米ドル)、2026年~2034年
図91:スペイン:医薬品安全性監視市場:販売額(百万米ドル)、2020年および2025年
図92:スペイン:医薬品安全性監視市場予測:販売額(百万米ドル)、2026年~2034年
図93:ロシア:医薬品安全性監視市場:販売額(百万米ドル)、2020年および2025年
図94:ロシア:医薬品安全性監視市場予測:販売額(百万米ドル)、2026年~2034年
図95:その他:医薬品安全性監視市場:販売額(百万米ドル)、2020年および2025年
図96:その他:医薬品安全性監視市場予測:販売額(百万米ドル)、2026年~2034年
図97:ラテンアメリカ:医薬品安全性監視市場:販売額(百万米ドル)、2020年および2025年
図98:ラテンアメリカ:医薬品安全性監視市場予測:販売額(百万米ドル)、2026年~2034年
図99:ブラジル:医薬品安全性監視市場:販売額(百万米ドル)、2020年および2025年
図100:ブラジル:医薬品安全性監視市場予測:販売額(百万米ドル)、2026年~2034年
図101:メキシコ:医薬品安全性監視市場:販売額(百万米ドル)、2020年および2025年
図102:メキシコ:医薬品安全性監視市場予測:販売額(百万米ドル)、2026年~2034年
図103:その他:医薬品安全性監視市場:販売額(百万米ドル)、2020年および2025年
図104:その他:医薬品安全性監視市場予測:販売額(百万米ドル)、2026年~2034年
図105:中東およびアフリカ:医薬品安全性監視市場:販売額(百万米ドル)、2020年および2025年
図106:中東およびアフリカ:医薬品安全性監視市場:国別内訳(%)、2025年
図107:中東およびアフリカ:医薬品安全性監視市場予測:販売額(百万米ドル)、2026年~2034年
図108:グローバル:医薬品安全性監視産業:SWOT分析
図109:グローバル:医薬品安全性監視産業:バリューチェーン分析
図110:グローバル:医薬品安全性監視産業:ポーターのファイブフォース分析

医薬品安全性監視、通称ファーマコビジランスとは、医薬品の有害作用(副作用)やその他の医薬品関連の問題を特定し、評価し、理解し、予防することを目的とした科学と活動を指します。患者様の安全を確保し、公衆衛生を向上させるために不可欠なプロセスであり、医薬品の治験段階から市販後まで、そのライフサイクル全体にわたって継続的に実施されます。
ファーマコビジランスにはいくつかの種類があります。まず、市販前ファーマコビジランスは、医薬品の臨床試験(治験)中に発生する有害事象の収集、評価、分析、および規制当局への報告を含みます。次に、市販後ファーマコビジランスは、医薬品が市場に出てから実施される活動で、主に以下の方法で行われます。医療従事者や患者様からの自発報告は、最も一般的な情報源の一つです。特定の医薬品を服用している患者群を追跡するコホート研究や、特定の有害事象を発症した患者群とそうでない患者群を比較する症例対照研究も行われます。また、医療記録データベースやレセプトデータなどを利用して大規模な安全性シグナルを検出するデータベース研究、特定の医薬品や患者群に対してより詳細な情報を収集する集中監視、そして特定のリスクを特定し最小化するためのリスク管理計画(RMP)の策定と実施も重要な活動です。
ファーマコビジランスの主な用途と応用は多岐にわたります。医薬品の新たな副作用や既知の副作用の頻度・重症度の変化を早期に発見し評価することで、医薬品の安全性プロファイルを確立し、そのベネフィットとリスクのバランスを継続的に評価します。得られた安全性情報は規制当局に報告され、必要に応じて添付文書の改訂や使用上の注意の追加が促されます。これにより、患者様が医薬品を安全かつ適正に使用できるよう情報が提供され、公衆衛生の保護に貢献します。また、治験段階での安全性評価を通じて、より安全な医薬品の開発にも寄与しています。
関連する技術としては、大量の安全性報告データを効率的に管理するためのデータベース管理システム(例:Argus Safety, ARISg)が不可欠です。データベース内の膨大なデータから新たな安全性シグナルを自動的に検出するデータマイニング・シグナル検出ツール(例:PRR, ROR)も活用されます。自由記述形式の副作用報告や医療記録から関連情報を抽出し、構造化されたデータに変換するために自然言語処理(NLP)技術が用いられます。さらに、人工知能(AI)や機械学習(ML)は、報告書の分類、シグナル検出の精度向上、リスク予測などに活用され始めています。電子カルテシステム(EHR)やレセプトデータは、大規模なリアルワールドデータ(RWD)として市販後調査や疫学研究に利用され、クラウドコンピューティングはグローバルなPV活動におけるデータ処理と共有を支援します。MedDRA(Medical Dictionary for Regulatory Activities)のような国際的に標準化された医学用語集は、副作用報告の統一と分析を可能にする重要な基盤技術です。